
| A. | 盐酸、纯碱、氣酸钾、氧化镁、二氧化硅 | |
| B. | 硝酸、烧碱、次氯酸钠、氧化钙、二氧化硫 | |
| C. | 次氯酸、消石灰、硫酸铵、过氧化钠、二氧化碳 | |
| D. | 氨基酸、过氧化钠、碱式碳酸铜、氧化铁、一氧化碳 |
分析 电离生成的阳离子全部是氢离子的化合物是酸;电离生成的阴离子全部是氢氧根离子的化合物是碱;能电离出金属阳离子(或铵根离子)和酸根离子的化合物是盐;能跟酸起反应,生成盐和水的氧化物叫碱性氧化物;酸性氧化物能与水作用成酸或与碱作用成盐和水的氧化物.
解答 解:A.盐酸、纯碱、氯酸钾、氧化镁、二氧化硅分别属于酸、盐、盐、碱性氧化物、酸性氧化物,故A错误;
B.硝酸、烧碱、次氯酸钠、氧化钙、二氧化硫分别属于酸、碱、盐、碱性氧化物、酸性氧化物,故B正确;
C.次氯酸、消石灰、硫酸铵、过氧化钠、二氧化碳分别属于酸、碱、盐、过氧化物、酸性氧化物,故C错误;
D.氨基酸、过氧化钠、碱式碳酸铜、氧化铁、一氧化碳分别属于氨基酸类、过氧化物、盐、碱性氧化物、不成盐氧化物,故D错误;
故选:B.
点评 本题是一道有关物质的分类的题目,熟记各种类型的物质的概念是解题的关键,注意过氧化钠不是碱性氧化物、一氧化碳不是酸性氧化物,题目较简单.


科目:高中化学 来源: 题型:解答题
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消去→加成→水解 | B. | 加成→消去→取代 | C. | 取代→消去→加成 | D. | 消去→加成→消去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应必然伴随发生能量变化 | |
| B. | 化学反应中能量变化的大小与反应物的状态有关 | |
| C. | 化学变化中的能量变化全部是由化学键变化引起的 | |
| D. | 能量变化是化学反应的基本特征之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉检验方法:加碘化钾变蓝 | B. | 蛋白质检验方法:浓硝酸或燃烧法 | ||
| C. | 蛋白质最终水解产物:葡萄糖 | D. | 淀粉最终水解产物:二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烷与NaOH溶液共热,在水解后的溶液中加入硫酸,再加入AgNO3溶液检验Cl- | |
| B. | 将电石和水反应后的气体通入溴水中,如果溴水褪色,证明乙炔和溴发生了反应 | |
| C. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| D. | 向苯酚浓溶液中滴入少量浓溴水可观察到白色三溴苯酚沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
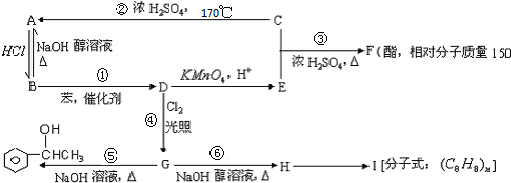



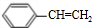 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$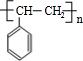 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-COOH | B. | CH2=CH-CH2-OH | C. | CH2=CH-COOH | D. | CH2=CH-COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
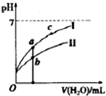 (1)25℃时,下列4种溶液.请回答下列问题.
(1)25℃时,下列4种溶液.请回答下列问题.| 物质 | H3PO2 | H2S | 一元酸HA |
| Kn | Kn=5.9×l0-2 | Kn1=9.1×l0-8 Kn2=l.l×l0-12 | Kn=l.1×1O-10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com