
| A. | 蒸馏 | B. | 分液 | C. | 过滤 | D. | 蒸发 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光束通过胶体时有丁达尔效应 | B. | 胶体粒子带电荷 | ||
| C. | 胶体是一种介稳性的分散系 | D. | 胶体粒子直径在1-100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60℃ | B. | 50℃ | C. | 70℃ | D. | 40℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分类方法应用广泛 | |
| B. | 纳米级粒子与胶体粒子的尺寸大致相当 | |
| C. | 胶体属于介稳体系 | |
| D. | 区分胶体与溶液的方法必须用丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
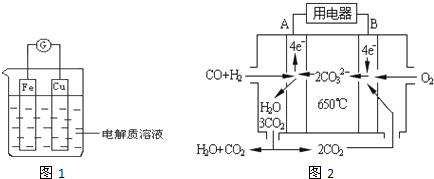
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com