
滴加新制氯水后,下列各组离子可能大量存在的是
A.Fe3+、Al3+、Cl-、NO
B.K+、Na+、I-、SO
C.Ag+、Ca2+、NH、NO
D.Na+、Ba2+、CO、SO
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二6月月考化学试卷(解析版) 题型:选择题
对于反应MnO2+4HCl(浓)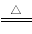 MnCl2+Cl2↑+2H2O,下列说法正确的是
MnCl2+Cl2↑+2H2O,下列说法正确的是
A.MnO2是还原剂 B.MnCl2是氧化产物
C.Cl2是氧化产物 D.H2O是还原产物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高二上学期期中化学试卷(解析版) 题型:选择题
有关晶体的下列说法中正确的是( )
A、分子晶体中共价键越强,熔点越高
B、原子晶体中分子间作用力越强,熔点越高
C、氯化钠晶体熔化时离子键发生断裂
D、金属晶体熔化时金属键未发生断裂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下学期期末化学试卷(解析版) 题型:填空题
Al及Al的合金在生活生产中有着广泛的应用
(1)航母升降机可由铝合金制造。
①Al元素在周期表中的位置是 ;
②Al—Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为: 。
(2)2015年11月首架C919大飞机总装下线,标志着我国跻身飞机研制先进国家行列。机身蒙皮使用的是第三代铝锂合金材料。下列不属于铝锂合金性质的是 (填字母)。
a.密度大 b.硬度大 c.抗腐蚀
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
2Al+4BaO 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3
常温下Al的金属性比Ba的金属性 (选填“强”“弱”)。
利用上述方法可制取Ba的主要原因是 。
a.高温时Al的活泼性大于Ba
b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定
d.Ba的沸点比Al的低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下学期期末化学试卷(解析版) 题型:选择题
下列关于浓硫酸的叙述正确的是
A.浓H2SO4使蔗糖炭化变黑,体现了浓H2SO4的氧化性
B.浓H2SO4使蓝色胆矾变成白色,体现了浓H2SO4的脱水性
C.浓H2SO4滴在润湿的蓝色石蕊试纸,试纸先变红,然后褪色,最后变黑,说明浓H2SO4具有酸性、氧化性和脱水性
D.100 mL 18 mol/L的浓H2SO4中加入足量的Cu并加热,被还原的H2SO4的物质的量为0.9 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:实验题
铝土矿是工业上制取铝的基本原料.为了除去铝土矿中的少量Fe2O3和SiO2等杂质制得纯净的Al2O3,化学兴趣小组设计探究实验,操作过程如图所示:
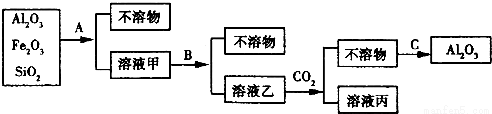
(1)操作过程中的试剂或方法:A加入的试剂______,B加入的试剂______,C采用的方法______。
(2)在溶液乙中通入过量CO2后发生反应的离子方程式为_______________。
(3)如果A、B互换,则通C02应改加______。
(4)如果A、B互换,将溶液乙蒸干并灼烧,所得固体产物的主要成分是______(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:选择题
镁、铝合金3 g与100mL稀H2SO4恰好完全反应,将反应后所得溶液蒸干,得无水硫酸盐17.4g,则原硫酸溶液的物质的量浓度为
A、1.5mol/L B、1mol/L C、2.5mol/L D.2mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A、依据铝热反应的原理,能发生反应 2Al+3MgO 3Mg+Al2O3
3Mg+Al2O3
B、镁铝合金既可以完全溶于过量盐酸又可以完全溶于过量的氢氧化钠的溶液
C、明矾可以做净水剂
D、常温下56克铁片投入足量浓硫酸生成NA个SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高二下学期期末考试化学试卷(解析版) 题型:选择题
某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH值升高,则该电解质可能是
A.NaOH B.H2SO4 C.AgNO3 D.Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com