
 自来水生成流程示意图
自来水生成流程示意图分析 (1)常用混凝剂为FeSO4•7H2O,被氧化、水解后生成Fe(OH)3;
(2)过滤需要漏斗、烧杯、玻璃棒;
(3)使用了氯气消毒,与水反应生成HCl、HClO;利用其具有强氧化性消毒;
(4)OH-会与钙、镁离子反应生成沉淀,影响阳离子交换树脂发挥作用;
(5)已知:2Mn2++4OH-+O2=2MnO(OH)2、MnO(OH)2+2I-+4H+=I2+Mn2++3H2O、I2+2S2O32-=2I-+S4O62-,可得关系式:O2~4S2O32-,以此计算.
解答 解:(1)亚铁离子不稳定,易被氧化生成铁离子,铁离子水解生成Fe(OH)3胶体,胶体具有吸附性而净水,则发生化学变化和物理变化;FeSO4•7H2O是常用的混凝剂,它在水中最终生成Fe(OH)3沉淀,故答案为:③;Fe(OH)3;
(2)过滤操作使用的玻璃仪器有玻璃棒、漏斗、烧杯等;故答案为:烧杯、漏斗、玻璃棒;
(3)氯气消毒是氯与水反应生成次氯酸消毒,原理是Cl2+H2O?HCl+HClO,臭氧、K2FeO4 具有强氧化性的物质可以代替氯气消毒,
故答案为:Cl2+H2O?HCl+HClO;①③;
(4)通过阴离子交换树脂后生成OH-,OH-会与钙、镁离子反应生成沉淀,影响阳离子交换树脂发挥作用,故先通过阳离子交换树脂再通过阴离子交换树脂,
故答案为:阳; 阴;
(5)已知:2Mn2++4OH-+O2=2MnO(OH)2、MnO(OH)2+2I-+4H+=I2+Mn2++3H2O、I2+2S2O32-=2I-+S4O62-,可得关系式:O2~4S2O32-,
n(S2O32-)=0.01mol/L×0.006L=6×10-5mol,则n(O2)=$\frac{1}{4}$×6×10-5mol=1.5×10-5mol,
m(O2)=1.5×10-5mol×32g/mol=48×10-5g=0.48mg,
则水中的溶解氧量为$\frac{0.48mg}{0.02L}$=24.0mg•L-1,
故答案为:24.0mg•L-1.
点评 本题考查物质的含量测定以及物质的分离、提纯实验方案的设计,为高频考点,侧重分析与应用能力、计算能力的综合考查,注意硬水的软化原理及关系式法在计算中的运用,题目难度中等.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 还原性强弱:F-<Cl-<I- | B. | 半径K+>Mg2+>Al3+>H+ | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
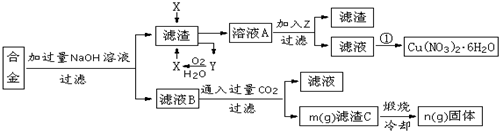
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素的原子半径:r(Z)>r(X)>r(Y)>r(W) | |
| B. | X、Y、Z、W形成的单质最多有6种 | |
| C. | 四种元素均可与氢元素形成18电子分子 | |
| D. | 四种元素中.Z的最高价氧化物对应水化物酸化最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
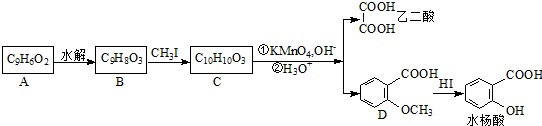
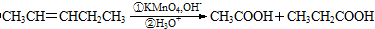
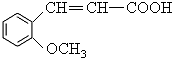 .
.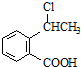 可以最终合成芳香内酯A,其中前两步的反应是
可以最终合成芳香内酯A,其中前两步的反应是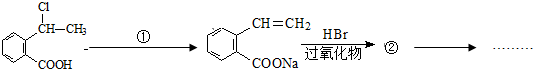
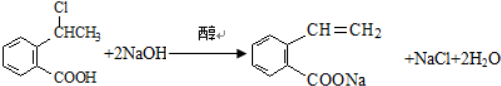 ,产物②的结构简式是
,产物②的结构简式是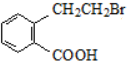 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝制容器可长期盛放酸性或碱性物质 | |
| B. | 甲烷会导致某些温泉有臭鸡蛋气味 | |
| C. | 太阳能的开发利用可降低碳排放量 | |
| D. | 塑料垃圾会造成水体富营养化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
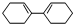 c.
c.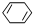 d.
d.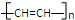
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$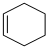 则要制备
则要制备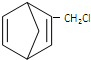 ,含共轭结构的原料可以是
,含共轭结构的原料可以是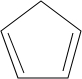 或
或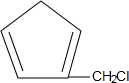 .(写结构简式)
.(写结构简式)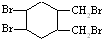 的合成路线(其他无机试剂任选).
的合成路线(其他无机试剂任选).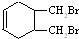 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
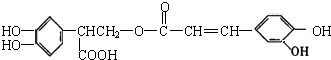
| A. | 迷迭香酸能使酸性高锰酸钾及溴的四氯化碳溶液褪色,属于芳香烃 | |
| B. | 迷迭香酸的分子式为C18H15O8,其在碱性条件下的水解反应叫皂化反应 | |
| C. | 迷迭香酸分子中含有5种官能团 | |
| D. | 1mol迷迭香酸跟H2反应,最多可消耗7molH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com