
| A、Ag++Cl-=AgCl↓的反应属于化合反应 |
| B、按照分散剂粒子的直径大小可将分散系分为溶液、胶体和浊液 |
| C、可以利用丁达尔效应区分胶体和溶液 |
| D、晶体硅是制造光导纤维的原料 |


科目:高中化学 来源: 题型:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
A、放电时正极反应为:FeO
| ||
| B、充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH- | ||
| C、放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 | ||
| D、标有“+”的接线柱充电时作阳极,放电时作正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、盐桥中的K+向负极移动 |
| B、负极电极反应方程式为:CH3OH-6e-+8OH-═CO32-+6H2O |
| C、每消耗1mol甲醇,需消耗33.6L标况下的氧气 |
| D、正极烧杯中溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水的导电性弱 |
| B、1 mol/L 的NH4Cl溶液pH<7 |
| C、0.1 mol/L 氨水溶液pH<13 |
| D、将pH=12的氨水稀释100倍后,pH>10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 除去Cl2中的HCl杂质 |
B、 稀释浓硫酸 |
C、 检查装置气密性 |
D、 实验室制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 粒子 | I2 | Br2 | IO3- |
| 物质的量/mol | 0.5 | 1.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 此图装置探究NaHCO3的热稳定性 |
B、 此图装置Cl2的收集 |
C、 此图装置向容量瓶中转移液体 |
D、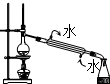 此图装置石油蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com