




���� ��1������T2�¶��£�0��2s��c��CO2������0.1mol/L�����v=$\frac{��c}{��t}$���㣬�ٸ�������֮�ȵ��ڻ�ѧ������֮�ȼ���v��N2����
�ڽӴ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ��
�۴ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣻
��2NO��g��+2CO��g��?2CO2��g��+N2��g��Ϊ���������С�ķ�Ӧ�����ԡ�S��0���ַ�Ӧ��һ�����������Է����У����ԡ�H��0���ݴ˷�����
��2���ٸ���ͼ2д���Ȼ�ѧ����ʽ�����ü���ȼ����д���Ȼ�ѧ����ʽ������1molˮ�������Һ̬ˮ����44kJд���Ȼ�ѧ����ʽ�������ø�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ��
����ΪCH4��g��+4NO��g��?2N2��g��+CO2��g��+2H2O��g��Ϊ�����������ķ�Ӧ�����Է�Ӧ��ϵѹǿ��СΪ0.5p���������Ϊԭ����2����ƽ�ⲻ�ƶ�����Ũ�ȼ�СΪԭ����$\frac{1}{2}$��
��3����װ����ԭ��أ�������һ����̼ʧ���ӷ���������Ӧ�������������õ��ӷ�����ԭ��Ӧ��ԭ��طŵ�ʱ���ӴӸ����������������������ƶ���һ����̼�ĺ���Խ��ԭ��طŵ�ʱ�����ĵ���Խ��
��� �⣺��1������ͼ��֪��T2�¶�ʱ2s����ƽ�⣬ƽ��ʱ������̼��Ũ�ȱ仯��Ϊ0.1mol/L����v��CO2��=$\frac{0.1mol/L}{2s}$=0.05mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��N2��=$\frac{1}{2}$v��CO2��=$\frac{1}{2}$��0.05mol/��L•s��=0.025mol/��L•s����
�ʴ�Ϊ��0.025mol/��L•s����
�ڽӴ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T����ƽ��ʱ��ͬ����c��CO2����T��S2�����´ﵽƽ������еı仯����Ϊ��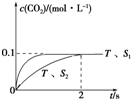 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��A������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮���淴Ӧ�������ʷ����仯��δ����ƽ�⣬��A����
B���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬Ϊ��С��ͼ����ʵ�ʷ��ϣ���B��ȷ��
C��t1ʱ�̺������̼��CO�����ʵ��������仯��t1ʱ��δ����ƽ��״̬����C����
D��NO����������Ϊ��ֵ��t1ʱ�̴���ƽ��״̬����D��ȷ��
�ʴ�Ϊ��BD��
��2NO��g��+2CO��g��?2CO2��g��+N2��g��Ϊ���������С�ķ�Ӧ�����ԡ�S��0���ַ�Ӧ��һ�����������Է����У����ԡ�H��0���������¶ȵĽ��ͣ�ƽ�������ƶ������Է�Ӧ��NO��ת���ʽ����ʴ�Ϊ�����÷�Ӧ��S��0����һ�����������Է����У����H��0��������ӦΪ���ȷ�Ӧ���¶Ƚ��ͣ�ƽ�������ƶ���
��2���ٸ���ͼ2���ɼ�������������Ϊ��945+498=1443KJ/mol���ų�����Ϊ��2��630=1260KJ/mol�����Ȼ�ѧ����ʽΪ2NO=O2+N2��H=-1260+1443=183KJ/mol�٣�����ȼ����Ϊ890kJ/mol����д���Ȼ�ѧ����ʽΪCH4��g��+2O2��g��=CO2��g��+2H2O��l������H=-890kJ/mol�ڣ�
H2O��g��=H2O��l������H=-44kJ/mol�ۣ��ɸ�˹���ɿ�֪��+�١�2-�ۡ�2���ɵ�Ŀ���Ȼ�ѧ����ʽ�����H=-810.1kJ/mol+183/mol��2-��44kJ/mol����2=-1168 kJ•mol-1��
�ʴ�Ϊ��-1168 kJ•mol-1��
����ΪCH4��g��+4NO��g��?2N2��g��+CO2��g��+2H2O��g��Ϊ�����������ķ�Ӧ�����Է�Ӧ��ϵѹǿ��СΪ0.5p���������Ϊԭ����2����ƽ�ⲻ�ƶ�����Ũ�ȼ�СΪԭ����$\frac{1}{2}$����CH4��ת���ʽ�=����N2�����ʵ���Ũ��Ϊ $\frac{1}{2}$c���ʴ�Ϊ��=��$\frac{1}{2}$c��
��3��A����װ����ԭ��أ�ͨ��һ����̼�ĵ缫a�Ǹ�����������һ����̼ʧ���ӷ���������Ӧ���缫��ӦʽΪ��CO+O2--2e-=CO2����A��ȷ��
B������ʱ�缫b��������O2-�ɵ缫b����缫a����B����
C����װ����ԭ��أ�ͨ��һ����̼�ĵ缫a�Ǹ�����ͨ������ĵ缫��������ԭ��طŵ�ʱ�����ӴӸ���aͨ������������缫b����C��ȷ��
D��һ����̼�ĺ���Խ��ԭ��طŵ�ʱ�����ĵ���Խ��D��ȷ��
�ʴ�Ϊ��B��
���� ���⿼���Ϊ�ۺϣ��漰��ѧƽ��ͼ��ѧ��Ӧ���ʡ�Ӱ�컯ѧƽ������ص�֪ʶ�㣬��Ϸ�Ӧ���Ȼ�ѧ����ʽ�����⣬����ԭ����������ϵ�ʧ���Ӽ���Ӧ���͡����ӵ��ƶ���������������4�����Ѷ��еȣ��Ƕ�֪ʶ���ۺ����á�ע�����֪ʶ���������գ�


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ũ���ὦ��Ƥ���ϣ�������NaOH��Һ��ϴ | |
| B�� | �ƾ���������������ʧ�𣬿���ˮ���� | |
| C�� | ������ˡ����˿��ñ�ˮ������ˮ����ֹʹ | |
| D�� | ��������Ա��Σ��ɼ�ʱ����Na2CO3��Һ�ⶾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N��10-2 mol/L | B�� | $\frac{N}{1.204��1022}$ mol/L | ||
| C�� | $\frac{N}{6.02��1021}$mol/L | D�� | $\frac{N}{6.02��1025}$mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10��b+2a-c�� | B�� | ��2b-c����0.3 | C�� | ��2b-a+c����0.3 | D�� | 10��b-c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2����ͨ��NaClO��Һ�У�������HClO�����֤��HClO������ | |
| B�� | ������SiO2��̼���η�Ӧ��������CO2���壬��˵����������Ա�̼��ǿ | |
| C�� | �������Ƶ�FeSO4��Һ�м���2��3��KSCN��Һ������Һ��Ѫ��ɫ����˵�������в���Fe2+������ΪFe3+ | |
| D�� | ��ͭƬ��Ũ�������ȣ�Ƭ�̺�ֹͣ���ȣ���ȴ���ٽ���ҺС�ĵ���ʢ������ˮ���ձ��У�����Һ����ɫ����˵��ͭ�ܱ�Ũ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��Ӧ������������ϵ����ͼ��ʾ����÷�ӦΪ���ȷ�Ӧ | |
| B�� | �����÷�Ӧ��Ƴ�ԭ��أ�пΪ���� | |
| C�� | ��ѧ��Ӧ���ʱ��뷴Ӧ����ʽ�ļ������й� | |
| D�� | ���������Ϊԭ��أ�����32.5gп�ܽ�ʱ�������ų�����һ��Ϊ11.2 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890.3 kJ•mol-1 | |
| B�� | ��N2��g��+3H2��g��2NH3��g����H=-92.4 kJ•mol-1�Ȼ�ѧ����ʽ��֪������Ӧ��ת��6NA��NAΪ�����ӵ�������ֵ������ʱ����Ӧ�ų�����������92.4kJ | |
| C�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3kJ•mol-1����H2SO4��KOH��Ӧ���к��ȡ�H=-57.3kJ•mol-1 | |
| D�� | ��101 kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ2H2��g��+O2��g��=2H2O��1����H=+571.6 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molN2��3molH2 | 2molNH3 | 4molNH3 |
| NH3��Ũ�ȣ�mol•L-1�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�akJ | ����bkJ | ����ckJ |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2++SO42-+Ba2++2OH-=BaSO4��+Fe��OH��2�� | |
| B�� | NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4��+Fe��OH��3��+NH3•H2O | |
| C�� | NH4++OH-=NH3•H2O | |
| D�� | 3NH4++Fe3++3SO42-+3Ba2++6OH-=3BaSO4��+Fe��OH��3��+3NH3•H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com