
 研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:分析 (1)直接标志:①速率关系:正反应速率与逆反应速率相等;②反应体系中各物质的百分含量保持不变.间接标志:①混合气体的总压强、总体积、总物质的量不随时间的改变而改变(m+n≠p+q);②各物质的浓度、物质的量不随时间的改变而改变;③各气体的体积、各气体的分压不随时间的改变而改变.
A.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)在密闭容器中m(混合气体)和v都不变,不能根据密度判断平衡状态;
B.混合气体m+n≠p+q反应体系中CO2的百分含量保持不变,达到平衡状态;
C.平衡常数只与温度有关,平衡常数变化,能判断达到平衡状态;
D.平均相对分子质量不变,由M(混合气体)=$\frac{m(混合气体)}{n(混合气体)}$可知,在密闭容器中能判断平衡状态;
(2)CO2也可在酸性水溶液中通过电解生成甲醇,在电解池的阴极CO2被还原生成甲醇;
(3)根据盖斯定律CO(g)+2H2(g)?CH3OH(g)△H3=△H1-△H2计算;
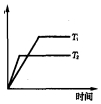
(4)①图中T2>T1,温度越高水蒸气的含量越少,平衡逆向移动,所以正反应是放热反应,所以△H1<0;
②A.降低反应温度,平衡正向移动,CO2平衡转化率增大;
B.在恒压密闭容器中,投料比不变,增加反应物的浓度,CO2平衡转化率不变;
C.增大CO2和H2的初始投料比,二氧化碳转化率降低,而氢的转化率增大;
D.混合气体中掺入一定量惰性气体,相当于减小压强,平衡逆向移动,二氧化碳转化率降低;
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I.
①容器的压强与起始压强之比为等于物质的量之比;
②根据v=$\frac{△c}{△t}$,求H2的平均反应速率;Kp=$\frac{P({H}_{2}O)•P(C{H}_{3}OH)}{P(C{O}_{2})•{P}^{3}({H}_{2})}$.
解答 解:(1)A.由ρ(混合气体)=$\frac{m(混合气体)}{V}$知,密闭容器中m(混合气体)和v都不变,比值不变,即ρ(混合气体)不变,密度不再改变不能达到平衡状态,故A错误;
B.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)反应前后体积不等,CO2的体积分数保持不变时,即反应体系中CO2的百分含量保持不变,达到平衡状态,故B正确;
C.平衡常数只与温度有关,绝热恒容密闭容器中发生反应,该反应的温度变化,所以平衡常数也变化,所以平衡常数能判断达到平衡状态,故C正确;
D.平均相对分子质量不变,由M(混合气体)=$\frac{m(混合气体)}{n(混合气体)}$,密闭容器中m(混合气体)不变,而n(混合气体)向正反应方向移动时减小,向逆反应方向移动时增大,故混合气体的平均相对分子质量不变,平衡不移动,能达到平衡状态,故D正确;
故选:BCD;
(2)CO2也可在酸性水溶液中通过电解生成甲醇,C元素化合价降低,被还原,应为电解池的阴极反应,电极方程式为CO2+6e-+6H+=CH3OH+H2O,
故答案为:CO2+6e-+6H+=CH3OH+H2O;
(3)由CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ;
CO2(g)+H2(g)?CO(g)+H2O(g)△H2=+41.2kJ•mol-8平衡常数K2 反应Ⅱ;
所以根据盖斯定律CO(g)+2H2(g)?CH3OH(g)△H3=△H1-△H2,K3=$\frac{{K}_{1}}{{K}_{2}}$,
故答案为:$\frac{{K}_{1}}{{K}_{2}}$;
(4)①图中T2>T1,温度越高水蒸气的含量越少,平衡逆向移动,所以正反应是放热反应,所以△H1<0,
故答案为:<;
②A.降低反应温度,平衡正向移动,CO2平衡转化率增大,故A正确;
B.在恒压密闭容器中,投料比不变,增加反应物的浓度,CO2平衡转化率不变,故B错误;
C.增大CO2和H2的初始投料比,二氧化碳转化率降低,而氢的转化率增大,故C错误;
D.混合气体中掺入一定量惰性气体,相当于减小压强,平衡逆向移动,二氧化碳转化率降低,故D错误;
故答案为:A;
(5)①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
c(初):1 3 0 0
c(变):a 3a a a
c(平):1-a 3-3a a a
所以$\frac{{P}_{0}}{P}$=$\frac{4}{4-2a}$;$\frac{{P}_{0}}{P}$=$\frac{2-a}{2}$,
故答案为:$\frac{2-a}{2}$;
②平衡后,混合气体物质的量为3.00mol,则反应的氢气的物质的量为1.5mol,v=$\frac{△c}{△t}$=$\frac{\frac{1.5mol}{1L}}{3h}$=0.500mol•L-1•h-1;
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
c(初):1 3 0 0
c(变):0.5 1.5 0.5 0.5
c(平):0.5 1.5 0.5 0.5
$\frac{P}{{P}_{0}}$=$\frac{1.5}{2}$,所以P=0.75P0,Kp=$\frac{P({H}_{2}O)•P(C{H}_{3}OH)}{P(C{O}_{2})•{P}^{3}({H}_{2})}$=$\frac{\frac{0.5}{3}×0.75{P}_{0}×\frac{0.5}{3}×0.75{P}_{0}}{\frac{0.5}{3}×0.75{P}_{0}×(\frac{1.5}{3}×0.75{P}_{0})^{3}}$=$\frac{27}{64{{P}_{0}}^{2}}$.
故答案为:0.500mol•L-1•h-1;$\frac{27}{64{{P}_{0}}^{2}}$.
点评 本题考查较为综合,涉及化学平衡的计算,平衡移动以及电化学等知识,为高考常见题型,侧重于学生的分析能力、计算能力的考查,注意电解池的工作原理等知识,题目难度中等,化学平衡计算为该题的难点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅原子和钠原子 | B. | 铜原子和氦原子 | C. | 碳原子和铝原子 | D. | 氧原子和碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
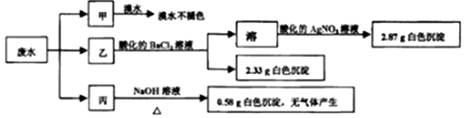
| A. | 废水可能含有Na+、K+、Fe3+ | |
| B. | 可能存在的离子用焰色反应进一步检验确认 | |
| C. | 废水一定含有Cl-、SO42-和Mg2+,且c(Cl-)=0.2mol•L-1 | |
| D. | 废水一定不含 SO32-、Cl-、NH4+、Na+、K+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 立方烷是新合成的一种烃,其分子呈正立方体结构.如图所示:
立方烷是新合成的一种烃,其分子呈正立方体结构.如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
| 0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
| 5min | 0.50mol | 0.50mol | ||
| 10min | 0.25mol | 0.75mol | ||
| 15min | 0.25mol | n1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 装置和试剂 | 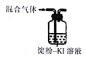 | 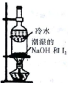 | 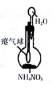 |  |
| 实验目的 | 检验NO2中混有溴蒸汽 | 分离潮湿的NaOH和I2 | 验证NH4NO3溶解吸热 | 制备和收集SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升温,逆反应速率减小 | B. | 加压,H2浓度减小 | ||
| C. | 增加H2,K减小 | D. | 该反应的正反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com