
| A£® | Ė®ČÜŅŗµ¼µēµÄŅ»¶ØŹĒ·Ö×Ó¾§Ģå | B£® | ČŪČŚĢ¬µ¼µēµÄŅ»¶ØŹĒĄė×Ó¾§Ģå | ||
| C£® | Ō×Ó¾§Ģå¹ĢĢ¬Ņ»¶Ø²»µ¼µē | D£® | ·Ö×Ó¾§ĢåČŪČŚĢ¬Ņ»¶Ø²»µ¼µē |
·ÖĪö A”¢¹²¼Ū»ÆŗĻĪļŗĶĄė×Ó»ÆŗĻĪļµÄĖ®ČÜŅŗ¶¼æÉÄܵ¼µē£»
B”¢ČŪČŚĢ¬Äܹ»µ¼µēµÄĪļÖŹÓŠ½šŹō¾§ĢåŗĶĄė×Ó¾§Ģ壻
C”¢Ō×Ó¾§Ģå¹č¹ĢĢ¬Ź±µ¼µē£»
D”¢·Ö×Ó¾§ĢåČŪ»ÆŹĒ·Ö×Ó¼ä×÷ÓĆĮ¦µÄ±ä»Æ£®
½ā“š ½ā£ŗA”¢¹²¼Ū»ÆŗĻĪļŗĶĄė×Ó»ÆŗĻĪļµÄĖ®ČÜŅŗ¶¼æÉÄܵ¼µē£¬ĖłŅŌ²»Ņ»¶ØŹĒ·Ö×Ó¾§Ģ壬¹ŹA“ķĪó£»
B”¢ČŪČŚĢ¬Äܹ»µ¼µēµÄĪļÖŹÓŠ½šŹō¾§ĢåŗĶĄė×Ó¾§Ģ壬ĖłŅŌČŪČŚĢ¬µ¼µēµÄŅ»¶ØŹĒĄė×Ó¾§Ģ壬¹ŹB“ķĪó£»
C”¢Ō×Ó¾§Ģå¹č¹ĢĢ¬Ź±µ¼µē£¬¹ŹC“ķĪó£»
D”¢·Ö×Ó¾§ĢåČŪ»ÆŹĒ·Ö×Ó¼ä×÷ÓĆĮ¦µÄ±ä»Æ£¬¶ųĪ¢Į£µÄÖÖĄą²»±ä£¬ĖłŅŌ·Ö×Ó¾§ĢåČŪČŚĢ¬Ņ»¶Ø²»µ¼µē£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹµÄµ¼µēŠŌÓėĪļÖŹĄąŠĶµÄ¹ŲĻµ£¬µ¼µēµÄĪļÖŹÖŠŗ¬ÓŠ×ŌÓÉŅĘ¶ÆµÄĄė×Ó»ņµē×Ó£¬×¢Ņā£ŗµ¼µēµÄĪļÖŹ²»Ņ»¶ØŹĒµē½āÖŹ£¬µē½āÖŹ²»Ņ»¶Øµ¼µē£¬ĪŖŅדķµć£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
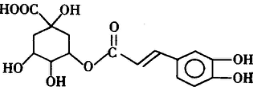
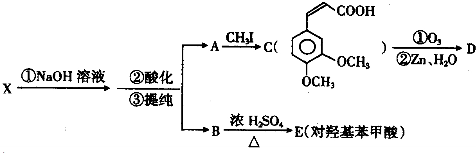
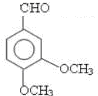 £»
£»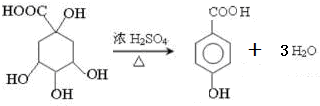 £»
£»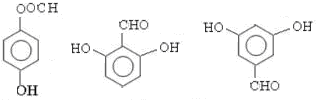 ČĪŅāŅ»ÖÖ£ØČĪŠ“Ņ»ÖÖ£©
ČĪŅāŅ»ÖÖ£ØČĪŠ“Ņ»ÖÖ£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņNa2SO3ČÜŅŗÖŠ¼ÓŃĪĖį£¬ÓŠĘųÅŻ²śÉś | |
| B£® | 0.1 mol•L-1ČÜŅŗµÄpH£ŗNaOH£¾LiOH | |
| C£® | Mg”¢AlÓėĶ¬ÅضČŃĪĖį·“Ó¦£¬Mgøü¾ēĮŅ | |
| D£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗHBr£¾HI |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
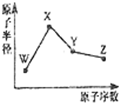 W”¢X”¢Y”¢ZŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹż±ä»ÆČēĶ¼ĖłŹ¾£®ŅŃÖŖWµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£»XŗĶNeŌ×ÓµÄŗĖĶāµē×ÓŹżĻą²īl£»YµÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£»ZµÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īĒ森ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
W”¢X”¢Y”¢ZŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹż±ä»ÆČēĶ¼ĖłŹ¾£®ŅŃÖŖWµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£»XŗĶNeŌ×ÓµÄŗĖĶāµē×ÓŹżĻą²īl£»YµÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£»ZµÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īĒ森ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ¶ŌÓ¦¼ņµ„Ąė×Ó°ė¾¶£ŗW£¾X | |
| B£® | ¶ŌÓ¦ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗY£¼Z | |
| C£® | »ÆŗĻĪļXZW¼Čŗ¬Ąė×Ó¼ü£¬ÓÖŗ¬¼«ŠŌ¹²¼Ū¼ü | |
| D£® | ZµÄĒā»ÆĪļŗĶXµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄČÜŅŗ¾łÄÜÓėYµÄŃõ»ÆĪļ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ąė×Ó | Mg2+ | Al3+ | ĪļÖŹ | Al£ØOH£©3 |
| æŖŹ¼³ĮµķŹ±µÄpH | 8.93 | 3.56 | æŖŹ¼ČܽāŹ±µÄpH | 8.04 |
| ĶźČ«³ĮµķŹ±µÄpH | 10.92 | 4.89 | ĶźČ«ČܽāŹ±µÄpH | 12.04 |
| A£® | 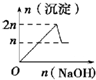 | B£® |  | C£® |  | D£® | 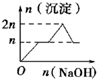 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
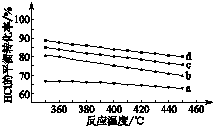 ÓĆCl2Éś²śŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśHCl£®ĄūÓĆ·“Ó¦4HCl£Øg£©+O2£Øg£©?2Cl2£Øg£©+2H2O£Øg£©æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ£®
ÓĆCl2Éś²śŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśHCl£®ĄūÓĆ·“Ó¦4HCl£Øg£©+O2£Øg£©?2Cl2£Øg£©+2H2O£Øg£©æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2Fe3++CuØT2Fe2++Cu2+ | B£® | Zn+2H+ØTZn2++H2”ü | ||
| C£® | 2H2+O2ØT2H2O | D£® | H++OH-ØTH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
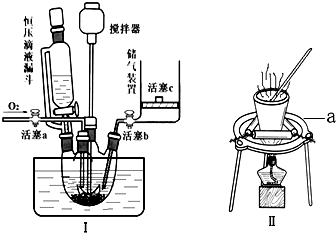
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com