
| A、1mol氢气为2克 |
| B、H2O的摩尔质量为18g?mol-1 |
| C、44克CO2的体积为22.4L |
| D、9.8g H2SO4含0.1NA个H2SO4分子 |
| m |
| M |


科目:高中化学 来源: 题型:
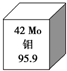 我国安徽发现了全国最大的钼矿,如图是钼元素的相关信息,下列有关钼的说法错误的是( )
我国安徽发现了全国最大的钼矿,如图是钼元素的相关信息,下列有关钼的说法错误的是( )| A、95Mo原子核内有53个中子 |
| B、95Mo原子核外有42个电子 |
| C、92Mo、95Mo、98Mo互为同位素 |
| D、92Mo、95Mo、98Mo的化学性质有较大的不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol羟基所含的电子总数为10NA | ||
B、标准状况下,1L正戊烷完全燃烧所生成的CO2分子数为
| ||
| C、4.2g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | ||
| D、1mol碳正离子(CH3+)所含的电子总数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去硫酸铜溶液中的硫酸亚铁以最终制备胆矾晶体:2Fe2++Cl2=2Fe3++2Cl- |
| B、在含有Mn2+的溶液中加入HNO3酸化,再加入PbO2,反应体系显紫红色,5PbO2+2Mn2++4H+=5Pb2++2MnO4-+2H2O |
| C、向Ba(OH)2溶液中加入过量的NH4HSO4溶液:Ba2++2OH-+NH4++H++SO42-=BaSO4+NH3?H2O+H2O |
| D、氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Al2(SO4)3═Al
| ||
| B、NaOH═Na++O2-+H+ | ||
C、NaHCO3═Na++H++CO
| ||
D、Na3PO4═3Na++PO
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com