
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是
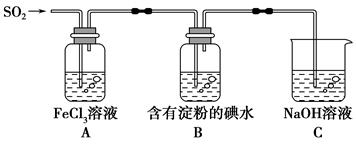
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液退色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色退去
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源:2016-2017学年贵州贵阳花溪清华中学高一上月考一化学卷(解析版) 题型:选择题
进行化学实验必须注意安全,下列说法不正确的是
A. 实验室中进行可燃性气体燃烧性质实验时,必须先验纯,后点燃
B. 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液
C. 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸
D. 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上期中化学试卷(解析版) 题型:填空题
(1)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如图(左)所示:原电池工作过程中OH-的作用是_______________;负极电极反应式为:_____________。若电路中转移电子数为0 .8NA,左侧溶液中pH________(填“增大”,“减小”,”不变”)(忽略溶液体积的变化),右侧的OH-物质的量变化量为_________。
.8NA,左侧溶液中pH________(填“增大”,“减小”,”不变”)(忽略溶液体积的变化),右侧的OH-物质的量变化量为_________。
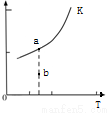
(2)CH4与H2O在隔绝空气、高 温和催化剂条件下反应:
温和催化剂条件下反应:
CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=m kJ·mol—1
CO(g)+3H2(g) ΔH=m kJ·mol—1
则反应的平衡常数表达式K=______________,K的大小与温度(T)的关系如上图(右)中曲线所示,则m__________0(填“>”“=”或“<”);改变某一条件,使状态从a点到达b点,若保持温度不变,反应再次达到平衡时,则CH4的转化率___________(填“增大”、“减小”、“不变”或“不确定”),反应的焓变(△H)将_______________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上期中化学试卷(解析版) 题型:选择题
下列各组离子在指定条件下,一定能大量共存的是
A.pH=1的无色溶液:Na+、Cu2+、NO3-、SO42-
B.能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl-
C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3-
D.能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学卷(解析版) 题型:填空题
研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1 反应Ⅰ
CH3OH(g)+H2O(g)△H1 反应Ⅰ
CO2(g)+H2(g) CO(g)+H2O(g)△H2 =+41.2kJ•mol-1 反应Ⅱ
CO(g)+H2O(g)△H2 =+41.2kJ•mol-1 反应Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
(1)研究证实,CO2可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式是_________________。
(2)从表中实验数据可以分析出,提高CO2转化成CH3OH的选择性的方法有______________。
(3)能说明反应Ⅱ已经达到平衡状态的是_____________。
A.混合气体的平均相对分子质量不变
B.混合气体的密度不变
C.v(H2)正>v(CO)正
D.n(CO)/n(H2)不变
(4)在恒容密闭容器中,由CO2和H2进行反应I合成甲醇,在其它条件不变的情况下,探究温度对化学平衡的影响,实验结果如图。
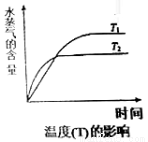
①△H1_________0(填“>”、“<”或“=”)
②有利于提高CO2平衡转化率的措施有___________(填标号)。
A.降低反应温度
B.投料比不变,增加反应物的浓度
C.增大CO2和H2的初始投料比
D.混合气体中掺入一定量惰性气体(不参与反应)
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I。
①充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为________(用a表示)。
②若经过3h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为____________(保留三位有效数字);平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数。则上述反应压力平衡常数KP为____________(用P0表示,并化简)。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学卷(解析版) 题型:选择题
化学中常用图像直观地描述化学反应的进程或结果,下列图像描述正确的是

A.图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化
B.图②表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(g)的影响,且甲的压强大
3C(g)+D(g)的影响,且甲的压强大
C.图③表示向Al2(SO4)3和MgSO4的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液体积的关系
D.图④表示在2 L的密闭容器中发生合成氨反应时N2的物质的量随时间的变化曲线,0~10 min内该反应的平均速率v(H2)=0.045 mol·L-1·min-1,从11 min起其他条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为d
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学卷(解析版) 题型:选择题
截止到2013年12月末,中国光伏发电新增装机容量达到10.66GW,光伏发电累计装机容量达到17.16GW,图为光伏并网发电装置电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。下列叙述中正确的是
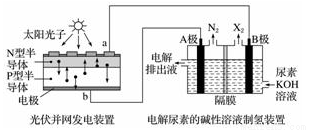
A.N型半导体为正极,P型半导体为负极
B.制氢装置溶液中电子流向:从B极流向A极
C.X2为氧气
D.工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上月考三化学试卷(解析版) 题型:计算题
有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀;滤液与4mol·L-1NaOH溶液反应,用去40mLNaOH溶液时恰好完全中和。试求:
(1 )混合液中H2SO4、HNO3的物质的量浓度各是多少?
)混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液稀释至80mL,加入4.48g铜粉共热时,收集到气体在标准状况下的体积为多少毫升?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上月考二化学卷(解析版) 题型:选择题
常温下,下列各组离子在指 定溶液中一定能大量共存的是
定溶液中一定能大量共存的是
A.pH=12的溶液: 、
、 、
、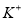 、
、
B.能使酚酞变红的溶液中: 、
、 、
、 、
、
C.0.1mol/L的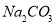 溶液中:
溶液中: 、
、 、
、 、
、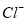
D.无色透明溶液中: 、
、 、
、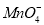 、
、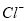
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com