
��һ��������ԭ��Ӧ����ϵ�У�����H2O��ClO-��CN-��HCO3-��N2��Cl-�������ʡ��ڷ�Ӧ�����в��ClO-��N2�����ʵ�����ʱ��仯��������ͼ��ʾ�������й��ж�����ȷ����
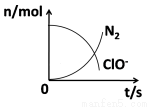
A����ԭ���Ǻ�CN-�����ʣ���������ֻ��N2
B����������ClO-����ԭ������HCO3-
C����ƽ���������뻹ԭ���Ļ�ѧ������֮��Ϊ4��1
D����״���£�������2.24LN2����ת�Ƶ�����ΪNA
 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ̩���н������߶���ѧ�����б���ѧ�Ծ��������棩 ���ͣ�ѡ����
Cl2��HCl�Ļ������ͨ��������NaOH��Һ����ַ�Ӧ����Һ�г�����OH���⣬����Cl����ClO���� ClO3�� �������������ӵ����ʵ���֮��Ϊ9:2:1����ԭ���������Cl2��HCl���֮��Ϊ
A��5:2 B��2:5 C�� 3:1 D��1:3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ�绯�и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˼ά�ǻ�ѧ�����г��õ�һ��˼ά�����������й����ӷ���ʽ��������ȷ����
��֪ | ���� | |
A | ��Fe����CuSO4��Һ�� Fe+Cu2+=Cu+Fe2+ | ��Na���뵽CuSO4��Һ�� 2Na+Cu2+=Cu+2Na+ |
B | ��Ca��ClO��2��Һ��ͨ������CO2 Ca2++2ClO-+CO2+H2O=CaCO3��+2HClO | ��Ca��ClO��2��Һ��ͨ������SO2 Ca2++2ClO-+SO2+H2O=CaSO3��+2HClO |
C | �ö��Ե缫���NaCl��Һ 2Cl-+2H2O | �ö��Ե缫���MgBr2��Һ 2Br-+2H2O |
D | ϡ������NaOH��Һ��Ӧ������ H++OH-=H2O | ϡHNO3��Ba��OH��2��Һ��Ӧ������ H++OH-=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й���Ԫ�ؼ��仯����ı�ʾ��ȷ����
A��������Ϊ17��������Ϊ20����ԭ�ӣ�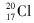
B��������(Cl�����Ľṹʾ��ͼ��
C���ȷ��ӵĵ���ʽ��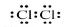
D������ϩ���ӵĽṹ��ʽ��H3C��CH2Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ�����������ȷ����
A��������Ľṹʽ��H��Cl��O
B������10�����ӵ���ԭ�ӵķ��ţ�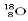
C��S2-�Ľṹʾ��ͼ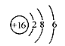
D��NH4Cl�ĵ���ʽ��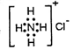
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
(8��)ȡNaHCO3��Na2O2�Ĺ�������x g����һ�ܱ������м�����250�棬��ַ�Ӧ���ų��������塣����Ӧ��Ĺ���ֳ���ȫ��ͬ�����ݣ�������һ��Ͷ�뵽������BaCl2��Һ�У����ɵõ�3.94g��������һ������������ˮ��������ų�������ˮ��Һ�л�����μ���ij���ʵ���Ũ�ȵ����ᣬ���������������������֮��Ĺ�ϵ����ͼ��ʾ���Իش��������⣺

��1������������ܹ������������ڱ�״���µ����Ϊ__________________L��
��2��������HCl�����ʵ���Ũ��__________________��
��3����Ӧ��Ĺ���ijɷ֣��ѧʽ��__________________��
��4��x=_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ǿ�ѧ�о�����Ҫ�������������ʷ����ȷ����
A��������ɱ�����ˮ�����ռС�մ�
B���ǵ���ʣ��Ҵ������Ȼ�̼��������������
C��ͬ�������壺����̿��C60��ʯīϩ�����ʯ
D���������ȼ���������Ȫˮ��ˮ������Ư��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
Zn��ԭSiCl4�ķ�Ӧ���£�
SiCl4(g) + 2Zn(l)  Si(s) + 2ZnCl2(g) ��H1
Si(s) + 2ZnCl2(g) ��H1
SiCl4(g) + 2Zn(g)  Si(s) + 2ZnCl2(g) ��H2
Si(s) + 2ZnCl2(g) ��H2
����˵����ȷ����
A��Zn(l)=Zn(g) ��H =1/2����H1-��H2 ��
B���ù�������̫���ܵ���ǽ���ѧ��ת��Ϊ����
C������Zn(g)��������H2���
D����ZnƬ��ͭƬ��ϡ���ṹ�ɵ�ԭ��أ�ZnƬ���������ݲ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��ÿ��2�֣���10�֣�����A��B��C��D��E����ǿ����ʣ�������ˮ�пɵ�������������ӣ��������Ӳ��ظ���
������ | H+ Na+ Al3+ Ag+ Ba2+ |
������ | OH- Cl- CO32- NO3- SO42- |
��֪��
������ | H+��Na+��Al3+��Ag+�� Ba2+ |
������ | OH���� Cl����CO32����NO3����SO42�� |
�� A��B����Һ�ʼ��ԣ�C��D��E��Һ�����ԡ�
�� A��Һ��E��Һ��Ӧ�����������г���������A��Һ��C��Һ��Ӧֻ������������������������ͬ����
�� D��Һ������������Һ��Ӧ���ܲ���������Cֻ����D��Ӧ����������
�Իش��������⣺
��1���ֱ�д��A��E�Ļ�ѧʽ��A ����2�֣�E ��2�֣�
��2��д��A��E��Ӧ�����ӷ���ʽ�� ����2�֣�
��3����֪��NaOH��aq��+HNO3��aq��=NaNO3��aq��+H2O��1������H =��Q kJ��mol-1��д��B��Cϡ��Һ��Ӧ���Ȼ�ѧ����ʽ ����2�֣�
��4����100 mL 0.1 mol��L-1 E��Һ�У���μ���40 mL 1.6 mol��L-1 NaOH��Һ�����յõ��������ʵ���Ϊ_____ mol����2�֣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com