
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。
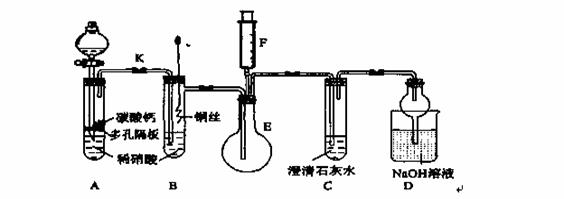
请回答有关问题:
(1)设计装置A的目的是
为达到此目的,应进行的操作是
(2)在完成(1)中的操作后,将装置B中铜丝插入稀硝酸,并微热之,观察
到装置B中的现象是
B中反应的离子方程式为:
(3)装置E和F的作用是
为实现此作用,其操作方法是
(4)装置D的作用是
【答案】
(1)利用生成的二氧化碳将整个装置内的空气赶尽,避免NO和氧气反应生成二氧化氮对气体产物的观察产生干扰;打开K,且打开分液漏斗活塞,当装置C中产生白色沉淀时,关闭K
(2)铜丝表面产生气泡,稀硝酸液面上仍为无色,溶液变为蓝色;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(3)验证无色气体为NO;将注射器F中的空气推入E中(或将E中的无色气体吸入到注射器中)
(4)吸收多余的氮氧化物,防止污染空气,兼有防止溶液倒流的功能
【解析】
(1)设计装置A的目的是利用生成的二氧化碳将整个装置内的空气赶尽,避免NO和氧气反应生成二氧化氮对气体产物的观察产生干扰; 为达到此目的,应进行的操作是打开K,且打开分液漏斗活塞,当装置C中产生白色沉淀时,关闭K。
(2)装置B中的现象是铜丝表面产生气泡,稀硝酸液面上仍为无色,溶液变为蓝色;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
(3)装置E和F的作用是NO;操作方法是将注射器F中的空气推入E中。
(4)装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有防止溶液倒流的功能


科目:高中化学 来源: 题型:
一定条件下,对于反应N2+3H2 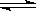 2NH3来说,下列反应速率中最快的是
2NH3来说,下列反应速率中最快的是
A.V(H2)=0.6mol/(L·min) B.V(N2)=0.3 mol/(L·min)
C.V(H2)=0.01 mol/(L·s) D.V(NH3)=0.5 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碳氢化合物的叙述正确的是 ( )。
A.碳氢化合 物的通式为CnH2n+2
物的通式为CnH2n+2
B.燃烧产物为二氧化碳和水的化合物一定是碳氢化合物
C.碳原子间以单键相连的烃是烷烃
D.碳氢化合物分子的相对分子质量一定是偶数
查看答案和解析>>
科目:高中化学 来源: 题型:
将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是
A.完全反应所需时间:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
查看答案和解析>>
科目:高中化学 来源: 题型:
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是:( )
A.正极反应式:Ag-e-+Cl-=AgCl↓ B.AgCl是还原产物
C.Na+不断向“水”电池的负极移动 D.每生成1 mol Na2Mn5O10转移2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,在不同的电解质溶液中可以组 成不同的电池。
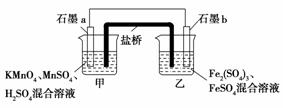
(1)①当电解质溶液为稀硫酸时,Fe电极是______(填“正”或“负”)极,其电极反应式为____________________________________________________________。
②当电解质溶液为NaOH溶液时,Al电极是______(填“正”或“负”)极,其电极反应式为________________________。
(2)若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______(填“正”或“负”)极,其电极反应式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com