
下列反应中前者属于取代反应,后者属于加成反应的是()
A. 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液退色
B. 苯与硝酸在一定条件下反应生成硝基苯;乙烯与溴的四氯化碳溶液反应
C. 乙烯与水生成乙醇的反应
D. 在苯中滴入溴水,水层褪色;乙烯与溴水反应
考点: 取代反应与加成反应.
分析: 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应;有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,根据定义分析解答.
解答: 解:A、甲烷和氯气混合光照一段时间后,甲烷中的氢原子被氯原子所代替生成氯代物,所以属于取代反应;乙烯使酸性高锰酸钾溶液褪色,是高锰酸钾和乙烯发生了氧化反应的结果,故A错误;
B、在浓硫酸和加热条件下,苯环上的氢原子被硝基取代生成硝基苯,所以属于取代反应;乙烯使溴的四氯化碳溶液褪色,是乙烯中的双键断裂,两个碳原子上分别结合两个溴原子,该反应属于加成反应,故B正确;
C、在一定条件下,乙烯中的双键断裂,一个碳原子上结合一个氢原子,另一个碳原子上结合羟基,生成乙醇,该反应属于加成反应,故C错误;
D、苯能萃取溴水中的溴而使水层无色,不是加成反应是萃取;乙烯使溴水褪色,是乙烯中的双键断裂,两个碳原子上分别结合两个溴原子,该反应属于加成反应,故D错误.
故选B.
点评: 本题考查了取代反应和加成反应的判断,难度不大,明确这两个概念的区别是解本题的关键.


科目:高中化学 来源: 题型:
类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。以下类推的结论中正确的是( )
A.SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色
B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气
C.SO2能使品红溶液褪色,故CO2也能使品红溶液褪色
D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
硝铝[Al(NO3)3]是一种常用媒染剂.工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3•9H2O]的流程如图甲:
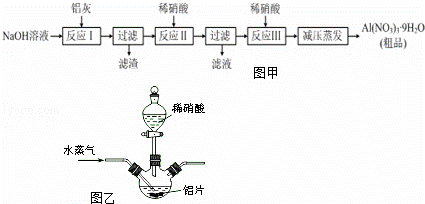
(1)写出反应Ⅰ的离子方程式: )(任写一个).
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是),可采取的措施为
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是.
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是.
(5)若用图乙所示实验装置制取Al(NO3)3,通入水蒸气的作用是.
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+3B═2C+2D在四种不同的情况下的反应速率如下,最快的是()
A. v(A)=0.15mol/(L•min) B. v(B)=0.6mol/(L•min)
C. v(c)=0.4mol/(L•min) D. v(D)=0.45mol/(L•min)
查看答案和解析>>
科目:高中化学 来源: 题型:
当铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率增大的是()
A. 不用稀硫酸,改用98%的浓硫酸
B. 加热
C. 适当增大稀硫酸的浓度
D. 不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
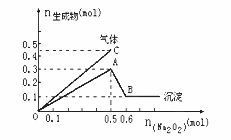
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )。
A. 1∶1∶2
B. 2∶2∶1
C. 1∶2∶2
D.9∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)1个NH4+的电子数为_______个,沸点PH3_______NH3(填大于、小于或等于)。
(2)NaNO2有毒,与食醋共熟会生成两种中学常见的氮氧化物气体,该反应的离子方程式为__________________________________________
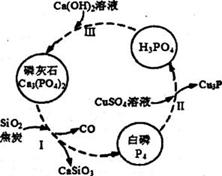
(3)磷及部分重要化合物的相互转化关系如下图所示。
①白磷(P4)的晶体类型为____________________。
②步骤I是白磷(P4)的工业生产方法。反应在高温条件下进行,其中SiO2的作用是用于造渣
(CaSiO3),焦炭的作用是作______________。 (填氧化剂或还原剂)
③不慎将自磷(P4)沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4
所能氧化的自磷(P4)的物质的量为___________
(4)人的牙齿表面有一层釉质,其组成为羟基磷灰石 Ca5(PO4)3OH(ksp=6.8×10﹣37)。人们常使用舍氟离子的牙膏防蛀牙,其中的氟化物可使羟基磷灰石转化为氟磷灰石Ca5(PO4)3F(Ksp=1.0×10﹣60)。写出该反应的离子方程式_____________________,该反应的平衡常数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
硅单质及其化合物在材料领域中一直扮演着主要角色.下列叙述中,不正确的是( )
|
| A. | 石英可用来制作工艺品 |
|
| B. | 硅单质可用来制造太阳能电池 |
|
| C. | 硅单质是制造玻璃的主要原料 |
|
| D. | 二氧化硅是制造光导纤维的材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com