
【题目】铝热反应是铝的一个重要性质.某校化学兴趣小组同学为了克服传统铝热反应纸漏斗易燃烧,火星四射等缺点,将实脸改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后补到“铁块”混合物.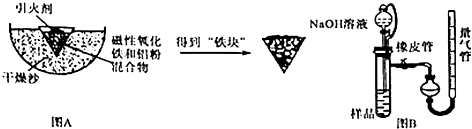
(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是 .
(2)该铝热反应的化学方程式为 .
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气体体积以测量样品中残留铝的百分含量.试回答下列问题:①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为 .
②量气管在读数时必须进行的步骤是 .
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为 .
④装置中分液漏斗上端和烧瓶用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用.如果装置没有橡胶管,测出铝的百分含量将会(填“偏大”或“偏小”).
【答案】
(1)蔗糖在浓硫酸中脱水并放出大量的热
(2)8Al+3Fe3O4 ![]() 4Al2O3+9Fe
4Al2O3+9Fe
(3)碱式滴定管;冷却至常温和调节量气管使左右液面相平;3.6%;偏大
【解析】解:(1)因为把浓硫酸加入到蔗糖中发生脱水并放出大量的热,可作引火剂,所以答案是:蔗糖在浓硫酸中脱水并放出大量的热;(2)Al还原Fe3O4生成Fe和Al2O3 , 由原子守恒可得化学方程式为8Al+3Fe3O4 ![]() 4Al2O3+9Fe,所以答案是:8Al+3Fe3O4
4Al2O3+9Fe,所以答案是:8Al+3Fe3O4 ![]() 4Al2O3+9Fe;(3)滴入足量NaOH溶液充分反应,测量生成气休体积以测量样品中残留铝的百分含量,由图可知,量气管测定氢气的体积,①因为该仪器盛放NaOH溶液,所以由碱式滴定管改装而成,所以答案是:碱式滴定管;②因为气体的体积受温度和压强影响,所以量气管在读数时必须进行的步骤是:冷却至常温和调节量气管使左右液面相平,所以答案是:冷却至常温和调节量气管使左右液面相平;③根据Al与NaOH溶液反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,m(Al)=n(Al)×27g/mol=
4Al2O3+9Fe;(3)滴入足量NaOH溶液充分反应,测量生成气休体积以测量样品中残留铝的百分含量,由图可知,量气管测定氢气的体积,①因为该仪器盛放NaOH溶液,所以由碱式滴定管改装而成,所以答案是:碱式滴定管;②因为气体的体积受温度和压强影响,所以量气管在读数时必须进行的步骤是:冷却至常温和调节量气管使左右液面相平,所以答案是:冷却至常温和调节量气管使左右液面相平;③根据Al与NaOH溶液反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,m(Al)=n(Al)×27g/mol= ![]() 3n(H2)×27g/mol=
3n(H2)×27g/mol= ![]() ×0.0448L÷22.4L/mol×27g/mol=0.036g,则铝的百分含量为
×0.0448L÷22.4L/mol×27g/mol=0.036g,则铝的百分含量为 ![]() ×100%=3.6%,所以答案是:3.6%;④如果装置没有橡胶管,烧瓶内压强增大,造成气体读数偏大,则铝的百分含量将会偏大,所以答案是:偏大.
×100%=3.6%,所以答案是:3.6%;④如果装置没有橡胶管,烧瓶内压强增大,造成气体读数偏大,则铝的百分含量将会偏大,所以答案是:偏大.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】使用酒精灯时,错误的操作是( )。
A. 用火柴点燃酒精灯 B. 熄灭酒精灯火焰时,用灯帽盖灭
C. 用酒精灯外焰给物质加热 D. 用燃着的酒精灯去点燃另一盏酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( ) 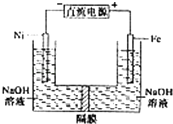
A.铁是阳极,电极反应为Fe﹣6e﹣+4H2O═FeO42﹣+8H
B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH﹣自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的正确叙述是( )
A.CH4O与C3H8O一定是同系物
B.同分异构体一定具有相似的化学性质
C.完全燃烧等质量的苯与苯乙烯,耗氧量相同
D.向溴乙烷中滴加硝酸银溶液,产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:
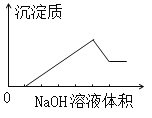
A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-浓度最小的是( )
A. 200mL 2mol/L MgCl2溶液 B. 300mL 5mol/L KCl溶液
C. 1000mL 2.5mol/L NaCl溶液 D. 250mL 1mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件的水溶液中可能大量共存的离子组是( )
A.c(H+):c(OH﹣)=1:2的溶液:K+、Al3+、H2PO4、ClO﹣
B.与Al反应生成H2的溶液:Na+、Ba2+、NO ![]() 、Cl﹣
、Cl﹣
C.中性溶液中:SO ![]() 、S2﹣、Fe3+、Cl、能大量共存
、S2﹣、Fe3+、Cl、能大量共存
D.能使红色酚酞变无色的溶液:K+、Ca2+、Cl﹣、HCO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机化合物中,一个碳原子与其他原子不能同时形成的化学键是( )
A.四个共价单键
B.一个双键,一个三键
C.两个单键,一个双键
D.一个单键,一个三键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是一种重要的化工原料.
(1)【问题1】绿矾晶体(FeSO47H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,某化学兴趣小组的同学设计了下列实验方案.实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
①方案1:取少量溶液,加入几滴试剂(写化学式),如果观察到的现象是溶液变血红色;实验结论:证明绿矾样品已被氧化.
②方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是 . 实验结论:证明绿矾样品完全被氧化.
③使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 .
④要从FeSO4溶液中得到绿矾晶体,必须进行的实验操作步骤:、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有(此空填序号)
A.蒸发皿 B.石棉网 C.烧杯 D.玻璃棒
(2)【问题2】灼烧绿矾的反应方程式:2(FeSO47H2O)═Fe2O3+SO2↑+SO3↑+14H2O工业上常通过高温分解FeSO4的方法制备Fe2O3 , 为检验FeSO4高温分解的气体产物中是否含有SO2和SO3 , 进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中.请回答以下问题: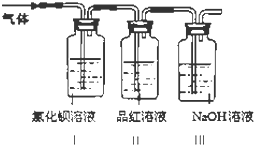
①装置I中氯化钡溶液中可观察到现象 . 若氯化钡溶液足量,将最后所得沉淀过滤、洗涤、烘干后称重为2.33克,则灼烧绿矾的过程中转移了mol的电子.
②装置II中试剂为品红溶液,其作用是
③装置III中试剂为NaOH溶液,其作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com