
| A. | 红外光谱法 | B. | 色谱法 | C. | 质谱法 | D. | 核磁共振氢谱法 |
分析 质谱法用于测定有机物的相对分子质量,红外光谱仪用于测定有机物的官能团,色谱法(chromatography)又称“色谱分析”、“色谱分析法”、“层析法”,是一种分离和分析方法,核磁共振氢谱用于测定有机物分子中氢原子的种类和数目.
解答 解:A、红外光谱仪能测定出有机物的官能团和化学键,故A正确;
B、色谱法(chromatography)又称“色谱分析”、“色谱分析法”、“层析法”,是一种分离和分析方法,在分析化学、有机化学、生物化学等领域有着非常广泛的应用,故B错误;
C、质谱法用于测定有机物的相对分子质量,不能测定出有机物的化学键和官能团,故C错误;
D、核磁共振氢谱用于测定有机物分子中氢原子的种类和数目,不能测定出有机物的化学键和官能团,故D错误;
故选A.
点评 本题考查了有机物的测定方法,较基础,了解各自方法的应用是解题的关键.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4 Cl2 H2 | B. | NO CO2 O2 | C. | NH3 N2 HCl | D. | H2S O2 SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用漫射散光照射甲烷与氯气的混合气体 | |
| B. | 乙烯通入溴水中 | |
| C. | 在镍做催化剂的条件下,苯与氢气反应 | |
| D. | 乙醇与酸性高锰酸钾溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将水加热,KW增大,pH不变 | |
| B. | 向水中加入少量的NaOH固体,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入少量的NH4Cl固体,平衡逆向移动,溶液呈碱性 | |
| D. | 向0.1mol/L的醋酸溶液中加入一定量的醋酸钠晶体,溶液中的c(OH-)增大,KW不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (4)(1)(3)(6)(3) | B. | (4)(3)(1)(6)(5)(3) | C. | (1)(3)(2)(6)(3) | D. | (4)(1)(3)(5)(6)(3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
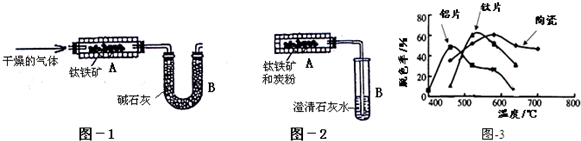
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com