
在0.5 mol·1-1MgCl2溶液中加入等体积的0.1 mol·1-1氨水,是否产生Mg(OH)2沉淀?
已知:Kb(NH3?H2O)=1.7×10-5mol?L-1,Ksp[Mg(OH)2]=5.6×10-12mol3?L-3。
有Mg(OH)2白色沉淀生成
【解析】
试题分析:氨水中存在电离平衡NH3?H2O NH4++OH-
NH4++OH-
又因为Kb=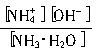
所以0.1mol?L-1氨水电离出的OH-的物质的量浓度为
[OH-]=
= mol?L-1
mol?L-1
=1.30×10-3mol?L-1
混合后溶液中镁离子和OH-的浓度分别是0.25mol/L和6.5×10-4mol?L-1
所以Qc=c(Mg2+)?c2(OH-)
=0.25×(6.5×10-4)2
=1.1×10-7mol3?L-3>Ksp[Mg(OH)2]
所以有沉淀生成。
考点:考查溶度积常数的有关计算
点评:本题是中等难度的试题,有利于培养学生的规范答题能力,也有利于培养学生灵活运用基础知识解决实际问题的能力。


科目:高中化学 来源: 题型:
A.v(O2)=0.01 mol·L-1·s-1 B.v(NO)=0.008 mol·L-1·s-1
C.v(H2O)=0.003 mol·L-1·s-1 D.v(NH3)=0.002 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2015届河北石家庄第二实验中学高一10月月考化学试卷(解析版) 题型:选择题
下列叙述中,错误的是( )
A.阿伏加德罗常数的符号为NA,其近似值为6.02×1023 mol-1
B.等物质的量的O2与O3,所含氧原子数相同
C.在0.5 mol Na2SO4中,含有的Na+数约是6.02×1023
D.摩尔是物质的量的单位
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高一上学期期末考试理科化学试卷 题型:选择题
用100 mL 10 mol·L-1的浓盐酸与足量的MnO2共热,充分反应后,被氧化的HCl的物质的量
A、小于0.5 mol B、等于0.5 mol
C、在0.5~1.0 mol之间 D、大于0.5 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com