
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为( )
A.CCl4与I2分子量相差较小,而H2O与I2分子量相差较大
B.CCl4与I2都是直线型分子,而H2O不是直线型分子
C.CCl4和I2都不含氢元素,而H2O中含有氢元素
D.CCl4和I2都是非极性分子,而H2O是极性分子
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:实验题
为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10mol/LKHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺为 。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、 。
(3) 完成并配平下列离子方程式:
C2O42- + MnO4—+ H+ = CO2↑+ Mn2+ +
(4)步骤③中判断滴定终点的方法是 。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(6)试样中H2C2O4·2H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省新高三零诊模拟理综化学试卷(解析版) 题型:选择题
电解质在溶液中的行为是化学研究的重要内容。下列有关溶液的叙述正确的是( )
A、常温下 pH为5的盐酸溶液稀释 1000倍后,pH 等于8
B、在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7
C、浓度均为0.1 mol/L的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者
D、等浓度的 CH3COOH与 KOH任意比混合:c(K+)+c(H+)= c(OH-)+c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二实验班下期中化学卷(解析版) 题型:推断题
下表为周期表的一部分,其中的编号代表对应的元素.
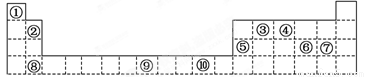
请回答下列问题:
(1)表中属于d区的元素是_____________(填编号)。
(2)写出元素⑨的基态原子的电子排布式_____________;
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为_____________对,其单质的电子式为_____________;
(4)元素④的氢化物的分子构型为_____________,中心原子的杂化方式为_____________;
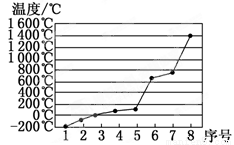
(5)第3周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表_____________(填元素符号);其中电负性最大的是_____________(填图中的序号)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二实验班下期中化学卷(解析版) 题型:选择题
下列关于分子组成表示为CxHy的烷、烯、炔烃说法不正确的是( )
A.当x≤4时,常温、常压下均为气体
B.y一定是偶数
C.分别燃烧1 mol,耗氧气为(x+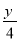 )mol
)mol
D.在密闭容器中完全燃烧,150℃时测得的压强一定比燃烧前压强大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二实验班下期中化学卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCI、HBr、HI的稳定性依次增强
D.CS2、H2O、C2H2都是直线型分子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二实验班下期中化学卷(解析版) 题型:选择题
已知短周期元素的离子,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径A>B>C>D
B. 原子序数D>C>B>A
C. 离子半径C3->D->B+>A2+
D. 单质的还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期末化学试卷(解析版) 题型:选择题
下列表示对应化学反应离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH-
B.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+
C.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O
D.过量氯气通入FeI2溶液中:3Cl2+2I- +4Fe2+=I2+4Fe3++4Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二下期末化学试卷(解析版) 题型:实验题
碳酸铈[Ce2(CO3)3]为白色粉末,难溶于水,主要用作生产铈的中间化合物。它可由氟碳酸铈精矿经如下流程制得。
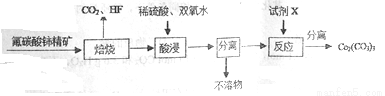
(1)如图是一种稀土元素铈(Ce)在元素周期表中的信息示意图。则铈原子的质子数是______,氟碳酸铈的化学式为CeFCO3,该化合物中,Ce的化合价为_____________;

(2)焙烧生成的铈化合物为二氧化铈(CeO2),其在酸浸时发生反应的离子方程式为______________;
(3)试剂X______________;
(4)已知298K时,Ksp[Ce(OH)4]=1×10-29,Ce(OH)4的溶度积表达式为Ksp=______________;为了使溶液中Ce4+沉淀完全,需调节pH为________以上;
(5)取某Ce(OH)4产品1.00g(质量分数为97%),加硫酸溶解后,用0.1000mol•L-1的FeSO4溶液滴定至终点(铈被还原成Ce3+)则需要滴加标准溶液的体积____________mL,若用硫酸酸化后改用0.1000mol•L-1
的FeCl2溶液滴定产品从而测定Ce(OH)4产品的质量分数,其它操作都正确,则测定的Ce(OH)4产品的质量分数__________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com