
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液的电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为____________、
______________;
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是__________,电解氯化钠溶液的总反应方程式为__________;
(3)若每个电池的甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C·mol-1,列式计算),最多能产生的氯气体积为__________ L(标准状况).
答案 (1)2O2+4H2O+8e-===8OH-,
CH4+10OH--8e-===CO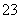 +7H2O
+7H2O
(2)H2
2NaCl+2H2O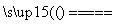 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3) ×8×9.65×104 C·mol-1=3.45×104 C 4
×8×9.65×104 C·mol-1=3.45×104 C 4
解析 本题考查了原电池、电解池的工作原理。(1)根据题意该燃料电池的总反应式为CH4+2O2+2OH-===CO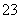 +3H2O,正极反应式为2O2+4H2O+8e-===8OH-,总反应式减去正极反应式,可得负极反应式为CH4-8e-+10OH-===CO
+3H2O,正极反应式为2O2+4H2O+8e-===8OH-,总反应式减去正极反应式,可得负极反应式为CH4-8e-+10OH-===CO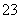 +7H2O。
+7H2O。
(2)三个池中前两个为串联的电源,通入CH4的电极为负极,与其相连的电极b为电解池的阴极,产生的气体为H2。
(3)1mol甲烷发生反应失去8mol电子。在串联电路中各电极转移电子数相等,故计算电子传递的电量,应用一个燃料电池的甲烷量计算,故理论上通过的电量为 ×8×96500 C·mol-1=3.45×104 C。甲烷的失电子数是等物质的量的Cl-失电子数的8倍,计算可得Cl2 4 L(标准状况)。
×8×96500 C·mol-1=3.45×104 C。甲烷的失电子数是等物质的量的Cl-失电子数的8倍,计算可得Cl2 4 L(标准状况)。


科目:高中化学 来源: 题型:
pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是( )
A.NaOH B.H2SO4
C.AgNO3 D.Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,划线物质是还原剂的是( )
A.Zn+H2SO4===ZnSO4+H2↑
B.Cl2+2NaBr===2NaCl+Br2
C.C+CO2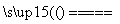 2CO
2CO
D.Fe2O3+2Al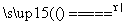 2Fe+Al2O3
2Fe+Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l)
ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l)
ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g)
ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2
C.Q3>Q2>Q1 D.Q2>Q1>Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com