
|
100 mL 6 mol/L H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可采取的措施有 | |
A. |
加入Na2SO4固体 |
B. |
加入H2O |
C. |
加入CuSO4固体 |
D. |
把锌粉换成锌粒 |
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源:湖北省武汉二中2011-2012学年高一上学期期中考试化学试题 题型:013
|
现有氧化铁和氧化铜的混合物m g,向其中加入100 mL 3 mol·L-1硝酸,恰好完全溶解,若m g该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为 | |
| [ ] | |
A. |
(m-1.6)g |
B. |
(m-2.4)g |
C. |
(m-3.2)g |
D. |
无法确定 |
查看答案和解析>>
科目:高中化学 来源:甘肃省天水市一中2009-2010学年高二上学期期末考试化学试卷(理) 题型:038
准确称取
6 g铝土矿(含Al2O3、Fe2O3、SiO2)样品放入盛有100 mL H2SO4的烧杯中充分反应后过滤,再向溶液中加入10 mol/L NaOH溶液,产生沉淀的质量m(g)与所加NaOH溶液的体积V(mol)关系如图所示.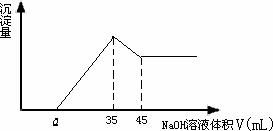
则①H2SO4溶液的物质的量浓度为:________.
②若a=2.75则铝土矿中各成分的质量百分含量是多少?
③a的取值范围是多少?a值越大,________含量越少.
查看答案和解析>>
科目:高中化学 来源:山东省莘县第二中学2009-2010学年高一下学期期末模拟考试化学试题 题型:022
短周期元素A、B、C、D中,0.5 mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4 g A的氧化物恰好与100 ml 0.2 mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外M层电子数目比K层多1个,C―比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子.
(1)A、D四种元素的名称分别是________、________;
(2)C元素在周期表中的位置是________;
(3)A~D四种元素最高价氧化物对应水化物中其中酸性最强的是________;
(4)向B、C两种元素形成的化合物的水溶液里逐滴滴入苛性钠溶液,写出有关离子方程式________;________.
查看答案和解析>>
科目:高中化学 来源:设计必修二化学人教版 人教版 题型:043
短周期元素A、B、C、D中,0.5 mol A元素离子得到6.02×1023个电子,被还原为中性原子,0.4 g A的氧化物恰好与100 mL 0.2 mol·L-1的盐酸完全反应.A元素原子核内质子数与中子数相等,B元素原子核外M层电子数比K层多1个,C-比A元素的离子多一个电子层,D元素原子核外L层比K层多2个电子,请完成下列问题:
(1)推断A、B、C、D四种元素的名称.
(2)画出C-和D原子的结构示意图.
(3)向B、C两元素形成的化合物的水溶液里逐滴滴入苛性钠溶液有什么现象?写出有关的化学方程式和离子方程式.
查看答案和解析>>
科目:高中化学 来源:吉林省长春市十一中2012届高三上学期期中考试化学试题 题型:013
|
将质量为m g的铁粉与铜粉的混合物,溶于100 mL 4 mol·L-1 HNO3溶液(过量),充分反应后所得还原产物为0.05 mol NO,再向所得溶液中加入足量的NaOH溶液至沉淀完全,则沉淀质量为 | |
| [ ] | |
A. |
5.52 g |
B. |
(m+6.8)g |
C. |
(m+2.55)g |
D. |
(m+12.0)g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com