
【题目】O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:反应①O3![]() O2+[O]ΔH>0平衡常数为K1;反应②[O]+O3
O2+[O]ΔH>0平衡常数为K1;反应②[O]+O3![]() 2O2ΔH<0平衡常数为K2;总反应:2O3
2O2ΔH<0平衡常数为K2;总反应:2O3![]() 3O2ΔH<0衡常数为K。下列叙述正确的是( )
3O2ΔH<0衡常数为K。下列叙述正确的是( )
A.升高温度,K增大B.K=K1+K2
C.适当升温,可提高消毒效率D.压强增大,K2减小
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】表所列各组物质中,物质之间通过一步反应就能实现如图所示转化且所给反应条件正确的是( )
序号 | X | Y | Z | 箭头上所标数字的反应条件 |
① | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
② | Na | Na2O2 | NaCl | ②加H2O |
③ | NO | NO2 | HNO3 | ③与C加热 |
④ | Al2O3 | NaAlO2 | Al(OH)3 | ④与NaOH |

A.①④B.①②C.③④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne 具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL2 mol·L-1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件完成下列问题:
(1)C元素位于第______周期第_____族,它的最高价氧化物的化学式为____。
(2)A元素是_____,B元素是_____,D元素是_____。(填元素符号)
(3)A与D形成稳定化合物的化学式是______,该化合物中存在的化学键类型为___,判断该化合物在空气中是否变质的简单方法是______。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予锂离子电池领域。LiFePO4(磷酸亚铁锂) 是锂离子电池的一种电极材料,可通过下列方法制备:
方法一:2FePO4(s)+Li2 CO3(s)+2C(s)2LiFePO4(s)+3CO(g)
(1)该反应的平衡常数表达式为_____。若在容积不变的容器中,上述反应达到平衡时,一氧化碳的浓度为amolL﹣1,再充入bmol一氧化碳,则平衡向_____方向移动,达到新平衡时,一氧化碳的浓度为_____。
(2)一定温度下,在2L密闭容器中发生上述反应。反应进行到20min时,容器内固体的质量减少了5.6g,则0~20min内一氧化碳的平均反应速率是_____。
方法二:LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与Li OH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
(3)氢氧化钠碱性比氢氧化锂碱性强,请用元素周期律知识说明理由_____。
(4)共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合,其原因是_____。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,放电时,负极为_____(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为_____。
LiFePO4,放电时,负极为_____(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示实验,回答问题:
(1)实验①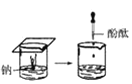 观察到的现象是________________________。实验②
观察到的现象是________________________。实验② 观察到的现象是________________________。
观察到的现象是________________________。
(2)实验③ 观察到的现象是________________________。实验④
观察到的现象是________________________。实验④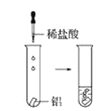 观察到的现象是________________________。
观察到的现象是________________________。
(3)由上述实验,你能得出的结论是________________________。
(4)请总结同周期元素金属性的变化规律__________,并用原子结构解释其原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是 ( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuSO4 | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.25℃时某溶液中水电离出的c(H+)=1.0×1012 mol·L1,其pH一定是12
B.某温度下,向氨水中通入CO2,随着CO2的通入, 不断增大
不断增大
C.恒温恒容下,反应X(g)+3Y(g) ![]() 2Z(g),起始充入3 mol X和3 mol Y,当X的体积分数不变时,反应达到平衡
2Z(g),起始充入3 mol X和3 mol Y,当X的体积分数不变时,反应达到平衡
D.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,该温度下加入等体积pH=10的NaOH溶液可使反应后的溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. pH=l 的溶液中:Ba2+、Fe3+ 、Cl-、SCN-
B. 能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32-
C. 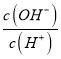 =10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D. 由水电离的c(H+)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com