
【题目】科学工作者研发了一种 SUNCAT 的系统,借助锂循环可持续合成氨,其原理如图所示。下列说法不正确的是

A.过程Ⅰ得到的 Li3N 中 N 元素为3 价
B.过程Ⅱ生成 W 的反应:Li3N+3H2O═3LiOH+NH3↑
C.过程Ⅲ中能量转化的形式:电能转变为化学能
D.过程Ⅲ涉及到反应:2H2O-4 e═O2↑+4H+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A.1molAl分别与足量的稀硫酸和稀硝酸反应转移电子数均为3NA
B.0.1molN4S4(结构如图所示)含有NA个S—N键
C.标准状况下,1mol甲基(—14CD3)所含的中子数为10NA
D.1molCH3COOC2H5在稀硫酸中水解可得到的乙醇分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S 为二元弱酸,20 ℃的 pKa1=6.89,pKa2=14.15(电离常数 K 的负对数-lg K=pK)。在20 ℃时,向 0.1 mol·L1 的 Na2S 溶液中缓慢通入 HCl(忽略溶液体积变化和 H2S 的挥发),在该过程中下列微粒物质的量浓度关系一定正确的是
A.溶液中 c(HS-)=c(S2-)时,c(S2-)+2c(H2S)<c(Cl-)
B.溶液呈中性时,c(HS- )+c(H2S)=c(Cl- )
C.溶液 pH=6.89 时,c(Cl- )>c(HS- )=c(H2S)>c(H+)>c(OH-)
D.溶液中 c(Cl-)=0.2 mol·L-1 时,c(OH-)+c(HS- )+c(S2-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用有机物甲可制备环己二烯(![]() ),其反应路线如图所示:
),其反应路线如图所示:

下列有关判断不正确的是
A.甲的分子式为 C6H12
B.乙与环己二烯互为同系物
C.上述流程发生的反应类型有取代反应、消去反应、加成反应
D.环己二烯与溴水 1:1 反应可得 2 种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示(图中 E1 表示无催化剂时正反应的活化能,E2 表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中 E1 表示无催化剂时正反应的活化能,E2 表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
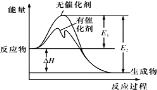
A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B.该反应中,反应物的总键能大于生成物的总键能
C.500℃、101kPa 下,将 1molSO2(g)和 0.5molO2(g)置于密闭容器中充分反应生成 SO3(g)放热 akJ,其热化学方程式为 2SO2(g) + O2(g)![]() 2SO3(g) ΔH<-2a kJ·mol-l
2SO3(g) ΔH<-2a kJ·mol-l
D.ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种常见金属组成的混合物A,在合适的条件下可按下图进行反应(部分产物和水省略),已知F为红褐色沉淀,请回答:

回答下列问题:
(1)混合物A的成分是_________(请填化学式)。
(2)反应①的离子方程式为:__________。
(3)反应②的化学方程式为:__________。
(4)写出E中加入过量NaOH的所有反应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
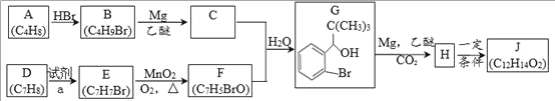
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如下:
已知:R-Br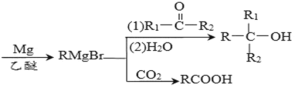
(1) A 的名称是_____,A分子中最多有_____个原子共平面。
(2) B 生成 A 的化学方程式_____。
(3) D 生成 E 的反应类型为_____
(4) F 的结构简式_____。
(5) J是一种酯,分子中除苯环外还含有一个五元环。写出 H 生成 J 的化学方程式_____(注明反应条件)。
(6)E![]()
![]() X,X 的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有_____种,写出其中核磁共振氢谱有五组吸收峰的结构简式_____。
X,X 的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有_____种,写出其中核磁共振氢谱有五组吸收峰的结构简式_____。
(7)利用题中信息和所学知识,写出以甲烷和化合物 D 为原料,合成![]() 的路线流程图_____(其它试剂自选)
的路线流程图_____(其它试剂自选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示:
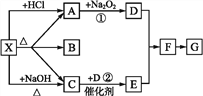
图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
(1)物质X可以是______,C是_________, F是______。
(2)反应①的化学方程式是_________,反应②的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经最新研究发现,NOx和SOx是形成雾霾天气的主要原因之一,因此研究NOx、SOx等大气污染物的妥善处理具有重要意义。
(1)为了消除NO造成的污染,通常采用一氧化碳和氢气进行催化还原NO。
已知:①N2(g)+O2(g)=2NO(g) ΔH=akJmol-1;
②2H2(g)+O2(g)=2H2O(l) ΔH=bkJmol-1;
③H2O(g)=H2O(l) ΔH=ckJmol-1。
写出H2与NO反应生成N2和水蒸气的热化学方程式:________________________。
(2)目前应用最广泛的烟气氮氧化物脱除技术是NH3催化还原氮氧化物(SCR)技术。反应原理如图所示:
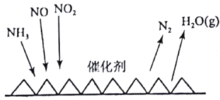
当NO2与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有12mol电子发生转移时,则参与反应的NO2的物质的量为________。
(3)T1温度时在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g) ΔH<0。实验测得:v正=v消耗(NO)=2v消耗(O2)=k正c2(NO)c(O2),v逆=v消耗(NO2)=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
2NO2(g) ΔH<0。实验测得:v正=v消耗(NO)=2v消耗(O2)=k正c2(NO)c(O2),v逆=v消耗(NO2)=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
时间/ | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
①从0~2s该反应的平均速率v(NO2)=________mol/(Ls)。
②T1温度时,上述反应的化学平衡常数K=________。
③若将容器的温度改变为T2时其k正=k逆,则T1________T2(填“![]() ”“
”“![]() ”或“
”或“![]() ”)。
”)。
(4)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图。
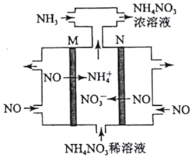
①N极的电极反应式为________________________。
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com