
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶解合金时收集到NO气体体积为2.24L(在标准状况) | |
| B. | 加入合金的质量不可能为9.6g | |
| C. | 沉淀完全时消耗NaOH溶液的体积为150mL | |
| D. | 参加反应的硝酸的物质的量为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
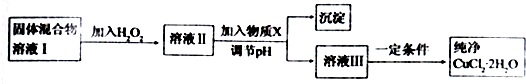
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲中负极反应式为Zn-2e-═Zn2+ | |
| B. | 乙中阳极反应式为Ag-e-═Ag+ | |
| C. | 丙中H+向碳棒方向移动 | |
| D. | 丁中电解开始时阳极产生黄绿色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凉拌青菜、土豆丝、馒头 | |
| B. | 虾仁白菜、红烧带鱼、酸菜炖猪蹄、萝卜汤 | |
| C. | 糖醋排骨、清蒸鲈鱼、米饭 | |
| D. | 酱牛肉、炒油菜、红烧豆腐、西红柿蛋汤、馒头 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 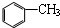 和 和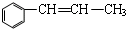 | |
| B. | 正丁烷和异丁烷 | |
| C. | 甲苯和二甲苯 | |
| D. | CH2═CH-CH═CH2和CH3-CH2-CH2-C≡CH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 其中碳的质量分数为$\frac{1}{13}$.碳碳键之间的夹角为1200.碳环呈平面正六边形结构,环上的碳碳之间的键完全相同.
其中碳的质量分数为$\frac{1}{13}$.碳碳键之间的夹角为1200.碳环呈平面正六边形结构,环上的碳碳之间的键完全相同.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
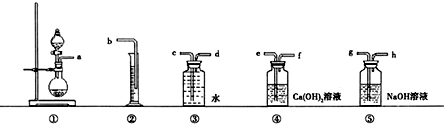
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com