
【题目】在下列条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Mg2+、I-、MnO4-
B.有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C.在强碱溶液中:Na+、K+、CO32-、NO3-
D.在强酸性溶液中:K+、HCO3-、SO42-、Cl-
科目:高中化学 来源: 题型:
【题目】
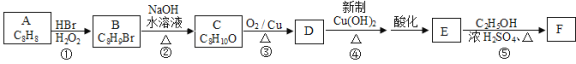
请回答下列问题:
(1)A是一种能与溴水反应使其褪色的芳香烃,其结构简式为 。
(2)在上述合成路线发生的反应中属于取代反应的是 (填反应编号)。
(3)反应①发生时若不加入H2O2,会生成较多的一种副产物。写出这种副产物的结构简式 。
(4)写出由C→D 、 E→F转化的化学反应方程式 、 。
(5)在化合物E多种同分异构体中,只含有一种含氧官能团,且能与FeCl3溶液发生显色反应的同分异构体有 种(不考虑羟基与碳碳双键直接连在一起的同分异构体),任写一种满足上述条件且核磁共振氢谱中有5个峰信号的同分异构体的结构简式 。
(6)按上述合成路线的表达形式,写出由![]() 制备
制备![]() 的合成路线。
的合成路线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某过碳酸钠(Na2CO4)中含有少量过氧化钠,甲、乙两位同学各称取一定质量的该样品,并用如下图所示仪器测定样品的纯度。
仪器的连接顺序,甲同学:⑤-⑧-③-⑦-④; 乙同学:⑤-③-②

已知:过碳酸钠(Na2CO4)、过氧化钠分别跟足量稀硫酸反应的化学方程式如下:
2Na2CO4 + 2H2SO4===2Na2SO4 + 2CO2↑+ O2↑+ 2H2O
2Na2O2 + 2H2SO4===2Na2SO4 + O2↑+ 2H2O
(1)甲同学想通过实验测得的数据是 ,他选用的装置 (填序号)是没有必要的。实验中甲同学测得气体体积为VL(20 ℃,1大气压),计算时他未将VL换算到标准状况,则他得到的Na2CO4的质量分数________。(填“偏高”或“偏低”)
(2)乙同学想通过实验测得的数据是 ,按他测得的数据计算出的实验结果有可能偏高,原因是 ,也有可能偏低,原因是 。
(3)为了测得准确的实验数据,请你将乙同学的实验设计进行改进,写出你所选用仪器的连接顺序(每种仪器最多使用一次,也可以不用) 。(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在。
(1)①可通过反应:NH3(g)+ Cl2(g)=NH2Cl(g)+ HCl(g)制备氯胺,己知部分化学键的键能:

则上述反应的△H=______________。
② NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为:_________________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) ![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400 ℃、400 ℃、T ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t 的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400 ℃、400 ℃、T ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t 的变化情况如下表所示:

①该反应为________(填“放热”或“吸热”)反应
②乙容器在200min达到平衡状态,则0~200 min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

A、B两点的浓度平衡常数关系:Kc(A)________Kc(B)(填“< ”或“> ”或“=”)。
A、B、C三点中NO2的转化率最高的是:__________(填“A”或“B”或“C”)点.
计算C点时该反应的压强平衡常数:Kp(C)=____________(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组根据SO2的性质进行如下相关实验研究。

【制备SO2】按照如图装置制备SO2。
(1)A试管中可观察到的现象是 ;SO2具有漂白性,试再举出两种漂白原理互不相同的物质 。
(2)若A试管中只加浓硫酸,加热过程中,导管b出口处的气体遇见潮湿的空气会有少量“酸雾”产生。推测b处出现酸雾的主要化学反应方程式为 。
(3)SO2尾气可以用浓氨水吸收。实验室制备NH3的化学方程式为__________;下列装置中宜用于NH3制备浓氨水的是 (填序号)。


【SO2浓度检测】
(4)学生用ME3 - SO2型电化学传感器测量试管B中SO2气体浓度,工作原理如右图。电极Ⅱ的反应式为 ;当通入VmL气体时,测得SO2浓度为amol/L。此时电解液中生成的n(H+)为 ;电化学传感器灵敏度受温度影响。若高于工作温度时,测得SO2,浓度可能偏低,其原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
Ⅰ.下表是某食品包装上的说明,表中列出了部分配料。请回答:

配料中,富含维生素的是_________(填序号,下同),属于调味剂的是__________,属于防腐剂的是 富含油脂的是___________。
Ⅱ.化学与生活密切相关。请判断下列说法是否正确(填“对”或“错”)。
(1)很多水果具有酸味,因此在生理上称为酸性食物。
(2)纤维素作为人类的营养物质,在人体内具有重要的生理功能。
(3)钢铁在潮湿的空气中被腐蚀,主要是在钢铁表面发生了电化学腐蚀的原因。
(4)装饰材料挥发出来的有机物如甲醛、苯等,是室内空气污染的重要来源之一。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳生活”是指减少能源消耗、节约资源,从而减少二氧化碳排放的生活方式。下列不符合“低碳生活”的做法是
A.节能灯代替白炽灯 B.太阳能热水器代替燃气热水器
C.纸巾代替棉手帕 D.环保袋代替一次性塑料袋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知常温下,Ksp[Fe(OH)3]=4.0×10-38, 在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:____________;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为_________molL-1
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的PH如下表
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述盐溶液中的阴离子,结合H+能力最强的是__________。根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,PH变化最大的是___________(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3) 下列说法不正确的是___ ___ ___ (填序号)
A.某温度下纯水中的c(H+)=10-6,故显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
C.相同温度下,0.1mol/LNH4Cl溶液中NH4+的浓度比0.1mol/L氨水中NH4+的浓度大
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com