
| A. | NH3$→_{催化剂,△}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$发烟硝酸 | |
| B. | Al2O3$\stackrel{盐酸}{→}$AlCl3(aq)$\stackrel{△}{→}$无水AlCl3$→_{熔融}^{电解}$Al | |
| C. | CuSO4(aq)$\stackrel{NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{蔗糖}$Cu2O | |
| D. | SiO2$→_{高温}^{Na_{2}CO_{3}}$Na2SiO3$\stackrel{盐酸}{→}$硅酸凝胶 |
分析 A.氨气催化氧化生成一氧化氮;
B.氧化铝溶解于盐酸中得到氯化铝溶液,氯化铝溶液蒸发得到氢氧化铝,不能得到氯化铝;
C.蔗糖是非还原性糖;
D.二氧化硅和碳酸钠高温反应生成硅酸钠和二氧化碳,硅酸钠和盐酸反应生成硅酸.
解答 解:A.氨气催化氧化生成一氧化氮,不能一步反应生成二氧化氮,二氧化氮溶于水得不到发烟硝酸,不能一步实现,故A错误;
B.氧化铝溶解于盐酸中得到氯化铝溶液,氯化铝溶液蒸发得到水解产物氢氧化铝,不能得到无水氯化铝,不能一步实现,故B错误;
C.蔗糖是非还原性糖,氢氧化铜浊液和蔗糖不能反应生成Cu2O,不能一步实现,故C. 错误;
D.二氧化硅和碳酸钠高温反应生成硅酸钠和二氧化碳,硅酸钠和盐酸反应生成硅酸沉淀,能一步实现,故D正确;
故选D.
点评 本题考查了物质性质和转化关系的分析,主要是氨气、氧化铝、二氧化硅、硫酸铜等物质性质的理解应用,注意反应条件和反应产物的判断,题目难度中等.


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应的离子方程式为CO32-+2H+═CO2↑+H2O | |
| B. | 与同浓度的盐酸反应,块状大理石的反应速率比粉末状的大 | |
| C. | CaCO3溶于盐酸是因为H+破坏了CaCO3的沉淀溶解平衡,使其ksp增大 | |
| D. | CaCO3与适量的盐酸恰好完全反应所得溶液中c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷的沸点低于甲烷,密度大于甲烷 | |
| B. | 相对分子质量相近的醇和烷烃,醇的沸点远高于烷烃 | |
| C. | 苯酚在任何温度下,均微溶于水 | |
| D. | 酯在碱性条件下的水解反应均为皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内消耗1molH2,同时生成2molHI | |
| B. | 每断裂AmolH-I,同时有$\frac{A}{2}$molH-H断裂 | |
| C. | 容器中压强不再变化 | |
| D. | 容器中混合气体的密度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉与稀盐酸的反应:Fe+2H+═Fe2++H2↑ | |
| B. | 硫酸铝溶液与氨水的反应:Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化铜与稀硫酸的反应:OH-+H+═H2O | |
| D. | 钠与水的反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2Al2(OH)4(CO3)3 | B. | Mg3Al2(OH)6(CO3)2 | C. | Mg3Al(OH)3(CO3)3 | D. | Mg3Al2(OH)8(CO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
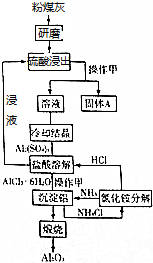 我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示:
我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com