

| 化学式 | Ag2SO4 | AgBr | AgCl |
| Ksp | 1.4×10-5 | 5.0×10-13 | 1.8×10-10 |
分析 (1)由工艺流程图可知,原电池中是SO2、Br2、H2O反应生成H2SO4、HBr;分离完全,硫酸中不含HBr,加入AgNO3溶液,根据沉淀颜色判断;
(2)原电池中电池总反应为:SO2+Br2+2H2O=H2SO4+2HBr,电解池中总反应为2HBr=H2+Br2,两式相加可得该工艺流程用总反应的化学方程式;
该生产工艺的优点:溴可以循环利用,获得清洁能源氢气,缺点是:生成过程有有毒物质,电解循环消耗能源大;
(3)依据沉淀转化的溶度积常数,结合氯化银和溴化银的溶度积常数计算得到需要溴离子的浓度.
解答 解:(1)取分离后的H2SO4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到无淡黄色沉淀产生,最终生成白色沉淀,说明分离效果较好,
故答案为:无淡黄色沉淀产生,最终生成白色沉淀;
(2)原电池中电池总反应为SO2+Br2+2H2O=H2SO4+2HBr,电解池中总反应为2HBr=H2+Br2,故该工艺流程用总反应的化学方程式表示为:SO2+2H2O=H2SO4+H2,该生产工艺的优点:溴可以循环利用,获得清洁能源氢气,
故答案为:SO2+2H2O=H2SO4+H2;溴可以循环利用,获得清洁能源氢气;
(3)某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol•L-1,加入等体积的溴化钠溶液,Ksp=c(Ag+)c(Br-)=5.0×10-13,Ksp=c(Ag+)c(Cl-)=1.8×10-10
,AgCl+Br-=AgBr+Cl-,$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=$\frac{Ksp(AgCl)}{Ksp(AgBr)}$,c(Br-)=$\frac{0.36×5.0×1{0}^{-13}}{1.8×1{0}^{-10}}$=10-3mol/L,
故答案为:10-3.
点评 本题考查电子式书写、原电池及电解池原理、元素化合物性质、化学工艺流程等,题目综合性较大,难度中等,是对知识的综合考查,注意基础知识的全面掌握.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②④ | C. | 只有①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .写出三种属于芳香烃类的A的同分异构体
.写出三种属于芳香烃类的A的同分异构体 、
、 、
、 .(不包括A,写结构简式)
.(不包括A,写结构简式) +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O;反应类型是氧化反应.C→E反应的化学方程是
+2H2O;反应类型是氧化反应.C→E反应的化学方程是 +NaOH $→_{△}^{水}$
+NaOH $→_{△}^{水}$ +NaCl;
+NaCl; ;反应类型是氧化反应.
;反应类型是氧化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.1mol•L-1的小苏打溶液与烧碱溶液等体积混合:2c(CO${\;}_{3}^{2-}$)+c(OH-)+c(HCO${\;}_{3}^{-}$)-c(H+)=0.1mol•L-1 | |
| B. | 浓度均为0.1mol•L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合c(SO${\;}_{4}^{2-}$)>c(Na+)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| C. | pH=12的氨水与pH=2的盐酸等体积混合c(Cl-)>c(NH${\;}_{4}^{+}$)>c(OH-)>c(H+) | |
| D. | 浓度均为0.1mol•L-1的醋酸溶液与氢氧化钠溶液等体积混合c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素处于最高价态,一定具有最强的氧化性 | |
| B. | 阳离子只有氧化性,阴离子只有还原性 | |
| C. | 还原剂失电子越多,还原性越强 | |
| D. | 在化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
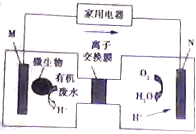 有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机物废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )
有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机物废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )| A. | 装置外电路中箭头的方向代表电流的方向 | |
| B. | 该装置为原电池,其中N为负极 | |
| C. | 标准状况下,N电极每消耗11.2L气体时会有4NA离子通过离子交换膜 | |
| D. | 若有机废水中含有葡萄糖,则M电极发生的电极反应为:C6H12O6+6H2O-24e-═6CO2+24H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数c>b | B. | 原子半径X<W | ||
| C. | 离子半径Y2-<Z- | D. | 离子的氧化性W3+>X+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | C-H | C=C | C-C | H-H |
| 键能/(KJ•mol-1) | 414.4 | 615.2 | 347.4 | 435.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com