
����Ŀ��ij�ֻ���ز�����ʯīϩ��أ��ɳ��5���ӣ�ͨ��2Сʱ��һ��ʯīϩ�����(2Li+S8=Li2S8)����ԭ��ʾ��ͼ��ͼ�������йظõ��˵������ȷ����
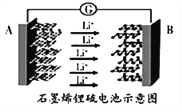
A. ����������н����б�������ߵĵ缫����
B. ���ʱA�缫Ϊ������������ԭ��Ӧ
C. ���ʱB�缫�ķ�Ӧ:Li2S8-2e-=2Li++S8
D. �ֻ�ʹ��ʱ���Ӵ�A�缫�����ֻ���·������B�缫���پ�����ص��������A�缫
���𰸡�D
��������A����λ�����ĵ缫����ʧȥ���ӵ����ʵ���Խ�࣬��õ��ĵ���Խ�࣬����Խ�ߣ�Li�����н���Ԫ����ԭ������С�Ľ��������Խ���������н����б�������ߵĵ缫���ϣ���A��ȷ��B��ԭ������������������ƶ�����ͼ��֪������Դʱ��BΪ������AΪ��������������ʧ���ӵ�������Ӧ�������������ʱ����Ϊ������������ԭ��Ӧ����B��ȷ��C��B�缫��S8�õ�������Li2S8����B�缫�ķ�Ӧ��2Li++S8+2e-�TLi2S8����C��ȷ��D������ֻ���ڵ缫�͵������ƶ������Ӳ����ڵ������Һ���ƶ�����D����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaOH��Һ�����ڶ�������Ĵ�����
��1��CO2���������壬����NaOH��Һ���յõ�Na2CO3��NaHCO3 �� ��Na2CO3�׳ƴ����CO32��ˮ���ʹ��ˮ��Һ�ʼ��ԣ�д��CO32����һ��ˮ������ӷ���ʽ �� ��֪25��ʱ��CO32����һ��ˮ���ƽ�ⳣ��Kh=2��10��4mol/L������Һ��c��HCO3������c��CO32����=20��1 ʱ����Һ��pH= ��
����ĭ�������ͨ��װ��NaHCO��Һ��Al2��SO4��3��Һ����д����������Һ���ʱ�����ӷ�Ӧ����ʽ ��
��2��������Ũ���ᷴӦ������NO2����NaOH��Һ���գ���Ӧ����ʽΪ��2NO2+2NaOH=NaNO3+NaNO2+H2O����0.2molNaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����ҺBΪ0��1molL��1CH3COONa��Һ����������Һ��c��NO3������c��NO2������c��CH3COO�����ɴ�С��˳��Ϊ����֪HNO2�ĵ��볣��Ka=7.1��10��4molL��1 �� CH3COOH�ĵ��볣��Ka=1.7��10��5molL��1������ʹ��ҺA����ҺB�� pH��ȵķ����� �� A������ҺA�м�����NaOH B������ҺA�м�����ˮ
C������ҺB�м�����NaOH D������ҺB�м�����ˮ
��3�������е�SO2���������꣬����������������Һ���գ�����SO2�Ĺ����У���Һ��H2SO3��HSO3����SO32��������ռ���ʵ���������a����pH�仯�Ĺ�ϵ��ͼ��ʾ�� 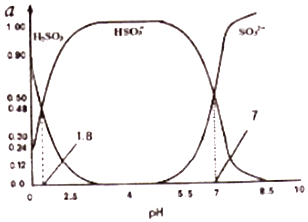
��ͼ��pH=7ʱ����Һ������Ũ�ȹ�ϵ��ȷ���� ��
A��c��Na+����2c��SO32������c��HSO3����
B��c��Na+��=c��SO32�� ��+c��HSO3����+c��H2SO3��
C��c��OH����=c��H+��+c��H2SO3��+c��HSO3����
D��c��Na+����c��HSO3������c��SO32�� ����c��H+��=c��OH����
��������ͼ�����ݣ���ӦH2SO3=2H++SO32����ƽ�ⳣ������ֵ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼȲ��ǵ����,�ֲ��Ƿǵ���ʵ���
A.ʳ��ˮB.�Ҵ�C.NaHSO4D.Ca(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧѡ��3�����ʽṹ�����ʡ�
�������ʯ�е�һ�֣�����Ҫ�ɷ�Ϊ��������-NaAI(Si2O6)��������Cr��Ni��Mn��Mg��Fe��Ԫ�ء��ش��������⣺
(l)��̬Crԭ�ӵĵ����Ų�ʽΪ____��Feλ��Ԫ�����ڱ���___ ����
(2)�������Ҫ�ɷֹ���ê�Ʊ�ʾΪ������Ļ�ѧʽΪ____����������Ԫ�ص�һ��������С�����˳����____��
(3)�ƺ������ǵ�������Ԫ�أ���ԭ�ӵ�������������ͬ��Ϊʲô�����۷е�Զ���ڸƣ�____��
(4)�ڹ������д���![]() �ṹ��Ԫ������Siԭ�ӵ��ӻ��������Ϊ____�������������n��ʾ��
�ṹ��Ԫ������Siԭ�ӵ��ӻ��������Ϊ____�������������n��ʾ��![]() �ֱ���3��������������3��
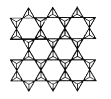
�ֱ���3��������������3��![]() �γɲ�״�ṹʱ����ͼ��ʾ��������Si��Oԭ�ӵ���Ŀ֮��Ϊ____��
�γɲ�״�ṹʱ����ͼ��ʾ��������Si��Oԭ�ӵ���Ŀ֮��Ϊ____��
��������һ���Si��Al�滻���仯ѧʽΪ____��
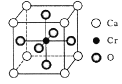
(5) Cr��Ca�����γ��־���������Եĸ�������������ṹ��ͼ��ʾ���þ���Ļ�ѧʽΪ____����Ca��O�ĺ˼����Ϊx nm����þ�����ܶ�Ϊ___ g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ����ķ�����ᴿ�������õķ����У��ٹ��ˡ�����������������ȡ���ݼ��ȷֽ�ȣ����и������ķ�����ᴿӦ����ʲô������������ţ�
��1����ȡ��ˮ�еĵ� ��
��2����ȥʳ����Һ�е�ˮ ��
��3��������ˮ ��
��4����ȥKC1�����к��е�����KClO3 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863 �ƻ���
(1)���������н�ǿ��ѡ���ԡ���֪:
��ӦI:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
��ӦII:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
д��NO �ֽ�����N2��O2���Ȼ�ѧ����ʽ______________________________________��
(2)N2OҲ�ɷֽ�����N2��O2�����ĸ������ܱ������а����±���Ӧ���������壬����2N2O(g)![]() 2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
���� | �ݻ�/L | ��ʼ���ʵ���/mol | ||
N2O | N2 | O2 | ||
I | V1 | 0.1 | 0 | 0 |
II | 1.0 | 0.1 | 0 | 0 |
III | V2 | 0.1 | 0 | 0 |
IV | 1.0 | 0.06 | 0.06 | 0.04 |
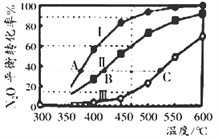
�ٸ÷�Ӧ�ġ�H_________0(�>������=������<��);
��ͼ��A��B��C ���㴦�����ڵ���ѹǿ���ɴ�С��˳����_____________________��
������IV��470����з�Ӧʱ����ʼ����:v(N2O)��____v (N2O)��(�>������=������<��)��
(3)��������ʱ�ᷢ����������������ӦI��II��Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���20L�ܱ������г�lmolNH3��2molO2�����һ��ʱ�����й����ʵ�����ϵ��ͼ:
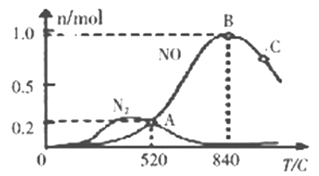
�ٸô����ڵ���ʱѡ��Ӧ________(�I����II��)��
��C���B����������NO�����ʵ����ٵ�ԭ�������_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ����У����������ǣ� ��
A.NaOH��ǿ�
B.CO2�������
C.H2SO4�����ᣩ
D.���ᣨ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ��˵����ȷ���ǣ������� 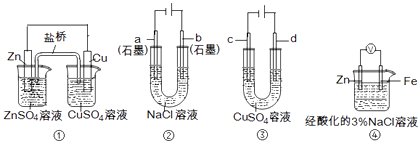
A.װ�â��У������е�K+����ZnSO4��Һ
B.װ�âڹ���һ��ʱ���a��������Һ��pH����
C.��װ�â۾���ͭʱ��c��Ϊ��ͭ
D.װ�â��е�����Zn����Fe��װ������Fe2+����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С�齫����������Ʊ���������ʵ�������һ�廯���,ʵ��װ����ͼ��ʾ������˵������ȷ����
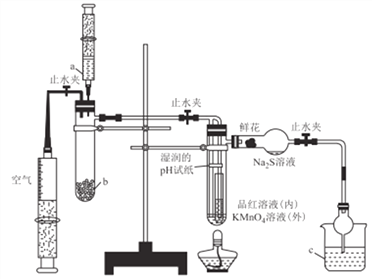
A. a��b��c������ʢװ70%����.Na2SO3���塢NaOH��Һ
B. ʵ��ʱ��ʪ���pH��ֽ���ʻ���Ʒ����Һ��KMnO4��Һ����ɫ��Na2S��Һ���ֵ���ɫ����
C. ����ƿ�֤��SO2ˮ��Һ������,SO2�������ԡ���ԭ�ԡ�Ư����
D. ��ȼ�ƾ��Ƽ���,��֤��SO2ʹƷ����Һ��ɫ���п�����,ʹKMnO4��Һ��ɫ�����п�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com