
| A. | 银氨溶液或新制Cu(OH)2均能检验糖尿病人尿液中的葡萄糖 | |
| B. | 在燃煤中加入适量生石灰,可以减少二氧化硫的排放 | |
| C. | 铜制品在潮湿环境中的腐蚀比干燥环境中快 | |
| D. | 生活中的水杯、奶瓶、食物保鲜膜等可以使用聚氯乙烯来制造 |
分析 A.葡萄糖含有醛基,可发生氧化反应;
B.二氧化硫为酸性氧化物,可与生石灰反应;
C.潮湿环境中易发生电化学腐蚀;
D.聚氯乙烯中的增塑剂对人体有害.
解答 解:A.葡萄糖含有醛基,可与银氨溶液或新制Cu(OH)2发生氧化反应,故A正确;
B.二氧化硫为酸性氧化物,可与生石灰反应,最终产物为硫酸钙,可减少污染性气体的排放,有效防治酸雨,故B正确;
C.潮湿环境中易发生电化学腐蚀,电化学腐蚀较化学腐蚀快,故C正确;
D.聚氯乙烯中的增塑剂对人体有害,且释放出氯化氢,一般不能用于生活中的水杯、奶瓶、食物保鲜膜等,可用聚乙烯材料,故D错误.
故选D.
点评 本题考查化学有机物的结构和性质,为高考常见题型,侧重于化学与生活、生产和环境的考查,难度不大,注意相关知识的积累.


科目:高中化学 来源: 题型:解答题
| 表1.几种砷酸盐的Ksp | |
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-9 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 7.2×10-21 |
| 表2.工厂污染物排放浓度及允许排放标准 | ||
| 污染物 | H2SO4 | As |
| 浓度 | 19.6g/L | 1.6g•L-1 |
| 排放标准 | pH6~9 | 0.5mg•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )
M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )| A. | X元素最高价氧化物对应水化物的酸性弱于Y元素的 | |
| B. | Y元素气态氢化物的稳定性大于Z元素的 | |
| C. | 元素Z在周期表中的位置为第2周期、VIA族 | |
| D. | M元素的氧化物既可以与强酸溶液反应,也可以与强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
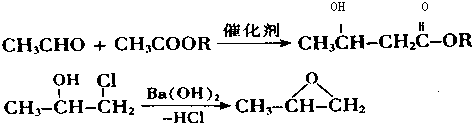
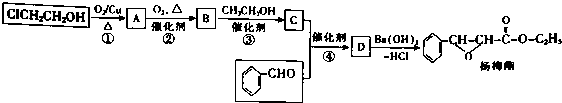
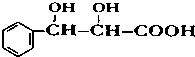 . 下列有关该物质的叙述中,正确的是CD.
. 下列有关该物质的叙述中,正确的是CD.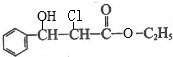 .
. 等.
等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 互为同分异构体 | B. | 均能与Na反应且产物相同 | ||
| C. | 均可发生取代反应和加成反应 | D. | 分子中共平面的碳原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
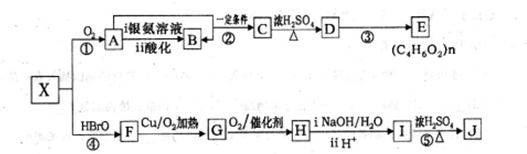

 .
. 查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| P>S | H->Li+ | KCl<Si | HClO3<HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 由图甲可知,升高温度醋酸钠的水解程度增大 | |
| B. | 由图乙可知,a点Kw的数值比b点Kw的数值大 | |
| C. | 由图丙可知,反应A(g)+B(g)=2C(g)是吸热反应 | |
| D. | 由图丁可知,反应C(金刚石,s)=C(石墨,s)的焓变△H=△H1-△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com