
下列说法不正确的是
A.任何化学反应都伴随着能量变化
B.放热反应的反应速率总是大于吸热反应的反应速率
C.离子化合物中一定含有离子键,可能含有共价键
D.强电解质与弱电解质的区别就是电解质在水溶液中是否完全电离
科目:高中化学 来源:2014-2015湖南省长沙市望城区高一上学期期末化学试卷(解析版) 题型:选择题
右图所示:2个甲分子反应生成1个丙分子和3个乙分子,对此下列判断不正确的是

A.化学反应中分子的种类发生了改变
B.该反应类型是分解反应
C.反应生成物只有丙属于单质
D.乙分子由有2个A原子构成
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省青岛市高三上学期期末考试化学试卷(解析版) 题型:选择题
以下关于下图说法正确的是
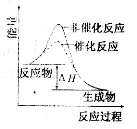
A.图表明催化剂可以改变反应的热效应
B.图表示某反应能量的变化与生成物状态无关
C.图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
D.图表明化学反应不仅遵循质量守恒定律,也遵循能量守恒
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
室温时,关于下列溶液的叙述正确的是
A.1.0×10—3mol/L盐酸的pH=3,1.0×10—8mol/L盐酸的pH=8
B.pH=a的醋酸溶液稀释l倍后,溶液的pH=b,则a>b
C.pH=12的氨水和pH=2的盐酸等体积混合,混合液的pH<7
D.1mLpH=l的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
若氧元素只有16O、18O两种核素,下列说法正确的是
A.16O和18O的物理性质和化学性质完全相同
B.通过化学反应可以实现16O与18O的相互转化
C.向2SO2(g)+O2(g) 2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中
2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中
D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:实验题
(19分) Na2S2O3可以用作氰化物的解毒剂,工业上常用硫化碱法制备Na2S2O3,反应原理为:2Na2S+Na2CO3+4SO2==3Na2S2O3+CO2,某研究小组在实验室模拟该工业原理制备Na2S2O3,实验装置如下:

Ⅰ.实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是_________________;
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合物,滤液经____________(填写操作名称)、过滤、洗涤、干燥,得到产品。
Ⅱ.[探究与反思]
(1)装置D的作用是检验装置C中SO2的吸收效率,则B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
(2)实验制得的Na2S2O3?5H2O样品中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
已知Na2S2O3?5H2O遇酸易分解:S2O32?+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
(3)为减少装置A中生成的Na2SO4的量,在不改变原有装置的基础上对原有实验步骤(2)进行了改进,改进后的操作是____________________。
Ⅲ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O32?+I2=== S4O62?+2I-
(1)滴定至终点时,溶液颜色的变化:___________________。
(2)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存
B.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:ClO-+CO2+ H2O =HClO+HCO3-
C.一定温度下,1L0.5mol·L-1NH4Cl溶液中与2L0.25mol·L-1NH4Cl溶液含NH4+物质的量相同
D.常温下水电离出c(H+)×c(OH-)=10-20的溶液中:Na+、ClO-、SO42-、NH4+可能大量共存
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中,能大量共存的是
A.含有NaClO的溶液中:K+,NH4+, Fe3+,Br-,SO32-
B.所含溶质为Na2S2O3的溶液:K+、SO42-、NO3-、H+
C.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入70 mL 4.0 mol/L盐酸中,充分反应后产生448 mL H2(标准状况),残留固体0.64 g。过滤,滤液中无Cu2+。将滤液加水稀释到200 mL,测得其中c(H+)为0.20 mol/L。则原混合物中单质铁的质量是
A.2.80g B.3.25g C.3.36g D.4.48g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com