
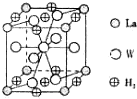
 ��A��B��C��D��E��F��G��W����ԭ���������������Ԫ�أ�ԭ��������С��30����Aԭ�ӵĺ������������Ӳ�����ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�E��Fͬ���壬G��Wͬ����ͬ����ԭ���������2����ش��������⣺
��A��B��C��D��E��F��G��W����ԭ���������������Ԫ�أ�ԭ��������С��30����Aԭ�ӵĺ������������Ӳ�����ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�E��Fͬ���壬G��Wͬ����ͬ����ԭ���������2����ش��������⣺���� A��B��C��D��E��F��G��W����Ԫ�ص�ԭ��������������Aԭ�ӵĺ������������Ӳ�����ȣ���AΪHԪ�أ�B�Ļ�̬ԭ����3����ͬ���ܼ����Ҹ��ܼ��еĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p2����BΪCԪ�أ�E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p4��1s22s22p63s2��D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��D��ԭ������С��E����ԭ�Ӻ�������Ų�ֻ��Ϊ1s22s22p4����DΪOԪ�ء���FΪMg��C��ԭ����������̼����֮�䣬��CΪNԪ�أ�E��Fͬ���壬��FΪCa��G��Wͬ����ͬ����ԭ���������2����GΪFe��WΪNi��
��� �⣺A��B��C��D��E��F��G��W����Ԫ�ص�ԭ��������������Aԭ�ӵĺ������������Ӳ�����ȣ���AΪHԪ�أ�B�Ļ�̬ԭ����3����ͬ���ܼ����Ҹ��ܼ��еĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p2����BΪCԪ�أ�E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�ԭ�Ӻ�������Ų�ʽΪ1s22s22p4��1s22s22p63s2��D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��D��ԭ������С��E����ԭ�Ӻ�������Ų�ֻ��Ϊ1s22s22p4����DΪOԪ�ء���FΪMg��C��ԭ����������̼����֮�䣬��CΪNԪ�أ�E��Fͬ���壬��FΪCa��G��Wͬ����ͬ����ԭ���������2����GΪFe��WΪNi��
��1��GΪFe����̬ԭ�ӵĺ�������Ų�Ϊ1s22s22p63s23p63d64s2���۵����Ų�ʽΪ��3d64s2��
ͬ������ԭ����������Ԫ�صĵ�һ�����ܳ��������ƣ���Ԫ��2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ���ͬ��������Ԫ�صģ��ʵ�һ������N��O��C��Nԭ�Ӻ���������Ų�Ϊ1s22s22p3����3�ֲ�ͬ�ܼ��ĵ��ӣ�CH3+��Cԭ���ӻ������ĿΪ3+$\frac{4-1-1��3}{4}$=3��Cԭ�ӵ��ӻ���ʽΪsp2�ӻ���
�ʴ�Ϊ��3d64s2��3��sp2�ӻ���
��2��a��B2A2����ΪC2H2����Ȳ�������к���1���Ҽ���2���м�����a��ȷ��
b��A2D2����ΪH2O2��˫��ˮ����֮���γ�������е����C2H2�ģ���b��ȷ��
c��H2O2������ÿ����ԭ�Ӻ���2�����õ��Ӷ��Һ���2���µ��Ӷԣ�������۲���Ӷ�����4����ԭ�Ӳ���sp3�ӻ���������ռ乹��Ϊչ����ҳ�ͣ���c����
d��ͬ����������ҵ縺�����ʵ縺��O��N��C����d��ȷ��
e��Ԫ��B��C������������ˮ����ֱ�Ϊ̼�ᡢ���ᣬ��������Ա�̼���ǿ����e��ȷ��
f��CaO���塢MgO�����Ϊ���Ӿ��壬�������������ͬ��þ���Ӱ뾶С�ڸ����ӵģ���MgO�ľ����ܸ�����MgO���۵��CaO�ĸߣ���f����
��ѡ��cf��
��3��FeCl3��Һ��KSCN��Һ��ϣ��õ�������������Ѫ��ɫ��Һ��������λ��Ϊ5�������Ļ�ѧʽ��K2[Fe��SCN��5]��
�ʴ�Ϊ��K2[Fe��SCN��5]��
��4��������Wԭ����ĿΪ1+8��$\frac{1}{2}$=5������������ĿΪ8��$\frac{1}{4}$+2��$\frac{1}{2}$=3����0.5mol W�ĺϽ����������Ϊ0.5mol��$\frac{3}{5}$=0.3mol������������������Ϊ0.3mol��22.4L/mol=6.72L��
�ʴ�Ϊ��6.72L��
���� �����Ƕ����ʽṹ�����ʵĿ��飬��Ŀ�漰��������Ų����ӻ���ʽ��ռ乹�͡��縺�ԡ�Ԫ�������ɡ��������������ʡ�������������ȣ��Ƕ����ʽṹ����֪ʶ�Ŀ��飬��ֿ�����ѧ���ķ���������������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
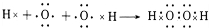
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ƺϽ��ǻ���� | |
| B�� | ���ƺϽ���Ͷ��һ����ˮ�пɵ���ɫ��Һ����n��Al����n��Na�� | |
| C�� | ���ƺϽ�Ͷ�뵽�����Ȼ�ͭ��Һ�У��϶���������ͭ����Ҳ������ͭ���� | |
| D�� | ��mg��ͬ��ɵ����ƺϽ�Ͷ�����������У��ų���H2Խ�࣬��������������ԽС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
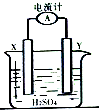 ijͬѧ������ͼ��ʾ��ͭ--пԭ���ʵ�飬��֪�������Һ��H+��X���ƶ���
ijͬѧ������ͼ��ʾ��ͭ--пԭ���ʵ�飬��֪�������Һ��H+��X���ƶ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
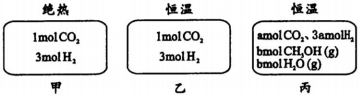
| A�� | �տ�ʼ��Ӧʱ���ʣ��ף��� | B�� | ƽ���Ӧ���ȣ��ף��� | ||
| C�� | 500���¸÷�Ӧƽ�ⳣ����K=3��102 | D�� | ��a��0����0.9��b��l |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
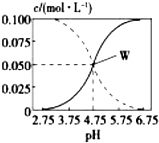 25��ʱ���ɴ���ʹ����ư�һ����������γɵ���Һʼ�ձ���c��CH3COOH��+c��CH3COO-��=0.1mol/L������Һ��c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ�������йظ���Һ����������ȷ���ǣ�������
25��ʱ���ɴ���ʹ����ư�һ����������γɵ���Һʼ�ձ���c��CH3COOH��+c��CH3COO-��=0.1mol/L������Һ��c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ�������йظ���Һ����������ȷ���ǣ�������| A�� | pH=5����Һ�У�c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | W������ʾ����Һ�У�c��Na+��=c��CH3COOH�� | |
| C�� | pH=3����Һ�У�c��H+��+c��Na+��+c��CH3COOH��=0.1mol/L | |
| D�� | ��ͼ�����ø��¶���CH3COOH�ĵ��볣��Ka=10-4.75 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ����ˮ����NO2�������3NO2+H2O=2HNO3+NO | |
| B�� | ����ʯ�Ҵ���й©��Һ�ȣ�2Ca��OH��2+2Cl2=CaCl2+Ca��ClO��2+2H2O | |
| C�� | Cu��ϡ���ᷴӦ��ȡ����ͭ��Cu+4H++2NO3-=Cu2++2NO2��+2H2O | |
| D�� | ��������ȥˮ�е����������Al3++3H2O?Al��OH��3�����壩+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �ҹ���ѧ����������������ű������Чҩ�����ض���ŵ��������ҽѧ���������صĽṹ��ͼ��ʾ���й������ص�˵������ȷ���ǣ�������
�ҹ���ѧ����������������ű������Чҩ�����ض���ŵ��������ҽѧ���������صĽṹ��ͼ��ʾ���й������ص�˵������ȷ���ǣ�������| A�� | �����ط���ʽΪC15H22O5 | |
| B�� | �����ط����ڵĹ��������ǶԸ�űԭ��ĺ��Ļ��� | |
| C�� | �������ܹ�����ˮ�ⷴӦ | |
| D�� | �����ط�������6������̼ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


| H2C204 | Ka1=5.36��10-2 | Ka2=5.35��10-5 |
| HF | Ka=6.32��10-4 | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com