
下列各项中的事实能用同一原理解释的是( )
A明矾和氯水都用于自来水的处理 B.干冰和碘化银都可用于人工降雨
C 向Fe(OH)3胶体和NaAlO2溶液中逐滴加盐酸,先出现沉淀,然后溶解
D 铁器和铝制容器都可以用来运输浓硫酸
科目:高中化学 来源: 题型:
下列叙述中,错误的是( )
A.阿伏加德罗常数的符号为NA,其近似值为6.02×1023 mol-1
B.等物质的量的O2与O3,所含氧原子数相同
C.在0.5 mol Na2SO4中,含有的Na+数约是6.02×1023
D.摩尔是物质的量的单位
查看答案和解析>>
科目:高中化学 来源: 题型:
已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量D,现将16 g A与70 g B的混合物充分反应后,生成2 mol D和一定量的C,则D的摩尔质量为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
往含0.2 mol KOH和0.1 mol Ca(OH)2的溶液中持续地通入CO2气体,当通入气体的体积为6.72 L(标准状况)时立即停止,则在这一过程中,溶液中离子的物质的量n和通入CO2的体积V的关系示意图正确的是(气体的溶解忽略不计) ( )
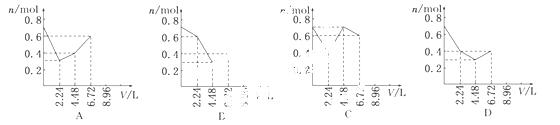
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、
S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
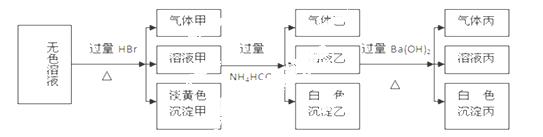
试回答下列问题:
(1)生成沉淀甲的离子方程式为: 。
(2)由溶液甲生成沉淀乙的离子方程式为 。
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(4)综上所述,该溶液肯定存在的离子有: 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列选项中,离子方程式书写正确的是( )
A.向硝酸银溶液中加入足量的氨水:Ag+ +2NH3·H2O = Ag(NH3)2+ + 2H2O
B. 向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-= 3Fe3++ 2H2O+NO↑[
C.泡沫灭火器的灭火原理:2Al3+ +3CO32-+3H2O = 2Al(OH)3↓+ 3CO2↑
D.用足量的氨水处理合成氨工业的尾气:SO2+ NH3·H2O = NH4+ + HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制得的Na2S2O3粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O的含量,一般采用在酸性条件下用酸性KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。称取1.28 g的粗样品溶于水,用0.40 mol/L的酸性 KMnO4溶液滴定,当溶液中S2O32—全部被氧化时,消耗KMnO4溶液体积20.00 mL。
① 滴定终点时的现象是________________________________________________________
② 写出该滴定反应的离子方程式__________________________________________________
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测定结果________(填“偏高”“偏低”或“不变”)
④经计算,产品中Na2S2O3·5H2O的质量分数为 ________
查看答案和解析>>
科目:高中化学 来源: 题型:
取一小块金属钠放在燃烧匙中加热,下列实验现象描述正确的是( )
①金属钠先熔化 ②在空气中燃烧,产生黄色火焰
③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质
A.①② B.①②③
C.③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四种元素中,第一电离能由大到小顺序正确的是
①.原子含有未成对电子最多的第二周期元素
②.电子排布为1s2的元素
③.周期表中电负性最强的元素
④.原子最外层电子排布为3s23p4的元素
A.②③①④ B.③①④② C.①③④② D.无法比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com