
分析 利用盖斯定律解答,从待求反应出发,分析待求反应中的反应物和生成物在已知反应中的位置,通过相互加减可得.
解答 解:已知:①O2(g)=O2+(g)+e-△H1=+1175.7kJ•mol-1
②PtF6(g)+e-=PtF6-(g)△H2=-771.1kJ•mol-1
③O2PtF6(S)=O2+(g)+PtF6-(g)△H3=+482.2kJ•mol-1
据盖斯定律,①+②-③得:O2(g)+PtF6(g)=O2PtF6(s)△H=-77.6 kJ•mol-1,
故答案为:-77.6.
点评 本题考查了盖斯定律在计算中的应用,题目难度中等,注意把握盖斯定律的含义,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
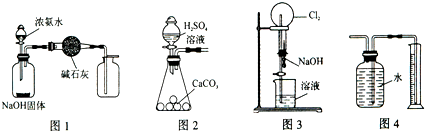
| A. | 用图1装置制取干燥纯净的NH3 | |
| B. | 用图2装置实验室制取大量CO2气体 | |
| C. | 用图3装置可以完成“喷泉”实验 | |
| D. | 用图4装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20 mL 10 mol•L-1的浓硝酸与足量铜加热反应转移电子数为0.2NA | |
| B. | 标准状况下,11.2L氦气中含有NA原子 | |
| C. | 在精炼铜或电镀铜的过程中,当阳极消耗铜32g时,转移电子数均为NA | |
| D. | 标准状况下,2.24L Cl2通入足量NaOH溶液中发生反应转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlO2-、Na+、HCO3-、K+ | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | K+、Al3+、Cl-、CO32- | D. | Cu2+、NH4+、I-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 为了测量NaHCO3和Na2CO3混合物中Na2CO3的质量分数,有人设计了如下的装置.准确称取混合物样品m g盛于试管B中并连接装置,其中C、D为玻璃管,C带有刻度,回答下面有关小题.
为了测量NaHCO3和Na2CO3混合物中Na2CO3的质量分数,有人设计了如下的装置.准确称取混合物样品m g盛于试管B中并连接装置,其中C、D为玻璃管,C带有刻度,回答下面有关小题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com