
已知氧化性Br2>Fe3+。FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:
a Fe2++b Br-+c Cl2→d Fe3++ e Br2+ f Cl-
下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是
A. 2 4 3 2 2 6 B. 0 2 1 0 1 2
C. 2 0 1 2 0 2 D. 2 2 2 2 1 4
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
漂白粉是一种常用的消毒剂。
(1)工业上生产漂白粉反应的化学方程式为__________________________________________
________________________________________________________________________,
漂白粉的有效成分为________。
(2)某探究小组从市场上购买了一袋包装破损的漂白粉,对该漂白粉的成分进行探究。根据下列试剂,设计实验方案,进行实验。请在答题卡上完成实验报告。
限选试剂:2 mol·L-1 NaOH溶液 、2 mol·L-1 HCl溶液、2 mol·L-1 HNO3溶液、0.5 mol·L-1 BaCl2溶液、0.01 mol·L-1 AgNO3溶液、澄清石灰水、石蕊试液、酚酞试液、蒸馏水。
、2 mol·L-1 HCl溶液、2 mol·L-1 HNO3溶液、0.5 mol·L-1 BaCl2溶液、0.01 mol·L-1 AgNO3溶液、澄清石灰水、石蕊试液、酚酞试液、蒸馏水。
| 实验步骤 | 预期现象与结论 |
| 步骤1:取适量漂白粉溶于足量蒸馏水,充分搅拌,静置,过滤,得沉淀和滤液。 | |
| 步骤2:向沉淀加入适量2 mol·L-1 HCl溶液,将产生的气体通入________________________________________________________________________ ________________________________________________________________________ | 现象:________________________________________________________________________ 结论:________________________________________________________________________ |
| 步骤3:取滤液分装A、B两支试管。向A试管,________________________________________________________________________ | 现象:溶液先变红色,然后褪色。 结论:________________________________________________________________________ |
| 步骤4:向B试管,________________________________________________________________________ ________________________________________________________________________ | 现象:产生白色沉淀。 结论:________________________________________________________________________ |
(3)探究小组为测定漂白粉中Ca(ClO)2的含量:称取漂白粉b g加水溶解后配制成100 mL溶液,准确量取25.00 mL于锥形瓶并加入足量盐酸和KI溶液,充分反应后,溶液中的游离碘用0.100 0 mol/L的Na2S2O3溶液滴定,滴定2次,平均消耗Na2S2O3溶液20.00 mL。则该漂白粉中Ca(ClO)2的质量分数为________________________________________________________________________。
(只列算式,不做运算,已知:Mr[Ca(ClO)2]=143;Ca(ClO)2+4HCl===2Cl2↑+CaCl2+2H2O,2Na2S2O3+I2===Na2S4O6+2NaI)
查看答案和解析>>
科目:高中化学 来源: 题型:
发展混合动力车是实施节能减排的重要措施之一。混合动力车的电动机目前一般使用的是镍氢电池。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理如图,其总反应式为: H2+2NiOOH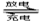 2Ni(OH)2
2Ni(OH)2
下列有关混合动力车的判断正确的是( )
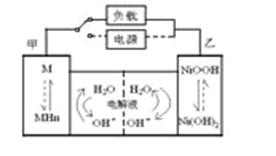
A.在上坡或加速时,每消耗22.4LH2,从电极甲流向电极乙的电子是2mol
B.在上坡或加速时,乙电极周围溶液的pH将减小
C.在刹车和下坡时,溶液中的K+向乙电极迁移
D.在刹车和下坡时,甲电极的电极反应式为2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
根据如图所示,下列判断错误的是( )
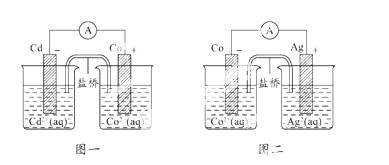
A.还原性:Co>Cd>Ag
B.还原性:Ag>Co>Cd
C .氧化性:Co2+>Cd2+>Ag+
.氧化性:Co2+>Cd2+>Ag+
D.氧化性:Ag+>Co2+>Cd2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述I和II均正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
| C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO |
| D | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①2FeCl3+2KI===2FeCl2+2KCl+I2 ②2FeCl2+Cl2===2FeCl3 ③I2+SO2+2H2O===H2SO4+2HI,判断下列物质的还原性由大到小的顺序是( )
A.I->Fe2+>Cl->SO2 B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.SO2>I->Fe2+>Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
________ +________
+________ +________
+________ →________
→________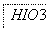 +________
+________
(2)整个过程中的还原剂是________.
(3)把KI换成KBr,则CCl4层变为________色;继续滴加氯水,CCl4层的颜色没有变 化.Cl2、HIO3、HBrO3氧化性由强到弱的顺序是________________________________.
化.Cl2、HIO3、HBrO3氧化性由强到弱的顺序是________________________________.
(4)加碘盐中含碘量为20 mg~50 mg/kg.制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2________L(标准状况,保留2位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热 反应 D.将锌粒投入Cu(NO3)2溶液
反应 D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)0.5 mol CH4的质量是________g,在标准状况下的体积为________L;含________个氢原子。
(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为________;配制300 mL 0.5 mol·L-1氯化钠溶液,需要1.5 mol·L-1的氯化钠溶液的体积是________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com