
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是________(填元素符号)。
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:
S2O +2I-===2SO
+2I-===2SO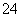 +I2
+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程:____________________________________________、
______________________________________________________(不必配平)。
科目:高中化学 来源: 题型:
肯定属于同族元素且性质相似的是 ( )。
A.原子核外电子排布式:A为1s22s2,B为1s2
B.结构示意图:A为 ,B为
,B为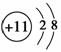
C.A原子基态时2p轨道上有1个未成对电子,B原子基态时3p轨道上也有1个未成对电子
D.A原子基态时2p轨道上有一对成对电子,B原子基态时3p轨道上也有一对成对电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于氧化还原反应的是____________,属于化合反应的是____________,属于分解反应的是________________________,属于置换反应的是______________,属于复分解反应的是______________。
①Cu2S+O2 2Cu+SO2
2Cu+SO2
②3O2 2O3
2O3
③Fe2O3+3CO===2Fe+3CO2
④2Na+2H2O===2NaOH+H2↑
⑤CaCO3 CaO+CO2↑
CaO+CO2↑
⑥2H2O2===2H2O+O2↑
⑦SO3+H2O===H2SO4
⑧2Fe+3Cl2 2FeCl3
2FeCl3
⑨H2SO4+2NaOH===Na2SO4+2H2O
⑩NaH+H2O===NaOH+H2↑
⑪IBr+H2O===HIO+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有a mol FeBr2的溶液中通入x mol Cl2。下列各项为通Cl2过程中溶液内发生反应的离子方程式,其中不正确的是( )
A.x=0.4a,2Fe2++Cl2===2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2===Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性Br2>Fe3+。FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为
aFe2++bBr-+cCl2—→dFe3++eBr2+fCl-
下列选项中的数字与离子方程式的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
A.2 4 3 2 2 6 B.0 2 1 0 1 2
C.2 0 1 2 0 2 D.2 2 2 2 1 4
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的总反应:3Fe2++2S2O +O2+xOH-===Fe3O4+S4O
+O2+xOH-===Fe3O4+S4O +2H2O,有关说法正确的是( )
+2H2O,有关说法正确的是( )
A.每转移1.5 mol电子,有1.125 mol Fe2+被氧化
B.x=2
C.Fe2+、S2O 都是还原剂
都是还原剂
D.每生成1 mol Fe3O4,反应中转移电子2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答下列问题:
(1)用软锰矿制备K2MnO4的化学方程式是_______________________________________。
(2)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为__________________。生成0.1 mol还原产物时转移电子__________个。KMnO4、K2MnO4和MnO2的氧化性由强到弱的顺序是__________________________________。
(3)KMnO4能与热的Na2C2O4(aq,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品 0.165 g,能与0.335 g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)[2014·天津理综,7(6)]KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于某无色溶液中所含离子的鉴别,下列判断正确的是( )
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
B.通入Cl2后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解时,可确定有SO 存在
存在
D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO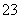 存在
存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com