
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | NaHC03固体 | Na2C03固体 | / | 加热 |
| B | Al2O3 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加热时,NaHC03固体易分解生成Na2C03固体,Na2C03固体较稳定,受热不易分解;
B.这两种物质都易溶于盐酸,但Al2O3能溶于NaOH溶液,Fe2O3不能溶于NaOH溶液;
C.Br2易溶于KOH溶液生成KBr、KBrO;
D.HCl极易溶于水,Cl2不易溶于饱和食盐水.
解答 解:A.加热时,NaHC03固体易分解生成Na2C03固体,Na2C03固体较稳定,受热不易分解,所以不能采用加热方法除杂,可以将固体溶于水然后通入过量二氧化碳,再在低温下蒸发溶液得到较纯净的碳酸氢钠固体,故A错误;
B.这两种物质都易溶于盐酸,但Al2O3能溶于NaOH溶液,Fe2O3不能溶于NaOH溶液,所以不能用稀盐酸除杂,故B错误;
C.Br2易溶于KOH溶液生成KBr、KBrO,引进新的杂质,所以不能用KOH溶液除杂,应该采用萃取方法分离提纯,故C错误;
D.HCl极易溶于水,饱和食盐水中含有Cl-而抑制氯气溶解,所以Cl2不易溶于饱和食盐水,可以用饱和食盐水除杂,采用洗气方法分离,故D正确;
故选D.
点评 本题考查物质分离和提纯,为高频考点,明确物质性质差异性是解本题关键,会根据物质性质差异性选取合适的分离提纯方法,注意:除杂时不能引进新的杂质,且操作简单易行,易错选项是D.


科目:高中化学 来源: 题型:选择题
| A. | CaCl2是中性干燥剂可以干燥NH3、SO2 | |
| B. | 检查病人胃病所用的钡餐,既可以用BaSO4,也可以用BaCO3 | |
| C. | 氮氧化物的大量排放是造成光化学烟雾的主要原因 | |
| D. | 雨水样品放置一段时间后,酸性增强的原因是因为溶解了空气中的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有4NA个电子转移时,放出890 kJ的能量 | |
| B. | 有NA个C-H键断裂时,放出890 kJ的能量 | |
| C. | 有2NA个H2O(l)生成时,放出890 kJ的能量 | |
| D. | 有NA个C、O间的共用电子对生成时,放出890 kJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
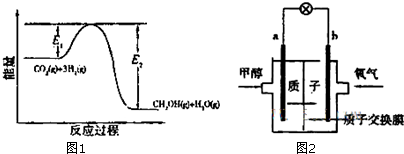
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4、C2H2、CO2 | B. | CH4、CHCl3、CO2 | C. | Cl2、H2、N2 | D. | NH3、H2O、CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘水加到溴化钠溶液中:2Br-+I2═2I-+Br2 | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 大理石溶于醋酸:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、SO42-、HCO3- | B. | Ba2+、K+、CO32-、NO3- | ||
| C. | I-、H+、Cl-、NO3- | D. | Al3+、K+、SO42-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com