
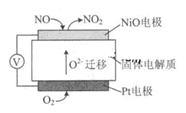
| A.NiO电极发生还原反应 |
| B.Pt电极是电池的负极 |
| C.NiO 电极的电极反应式:NO—2e—+O2—=NO2 |
| D.该电池在标准状况下,若Pt电极消耗2.24L O2,NiO电极电极产生2.24LNO2气体 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.Al片均作阴极 |
| B.电解质溶液的pH均逐渐升高 |
| C.Cu片上均有气泡放出 |
| D.电路中流过等物质的量的电子时,放出等体积的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应中MnO2是还原剂 |
| B.Ag的还原性比Na2Mn5O10强 |
| C.该反应中MnO2具有催化作用 |
| D.每生成1 mol Na2Mn5O10转移1 mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg为电池的正极 |
| B.负极反应为AgCl+e-=Ag+Cl- |
| C.不能被KCl溶液激活 |
| D.可用于海上应急照明供电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌为负极,氧化银为正极 |
| B.锌为正极,氧化银为负极 |
| C.原电池工作时,负极区溶液pH增大 |
| D.原电池反应的化学方程式为Zn+Ag2O+H2O=Zn(OH)2+2Ag |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


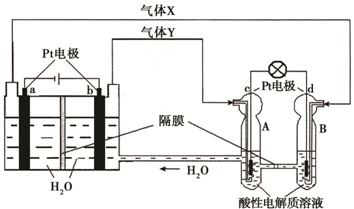
| A.铝 | B.石墨 | C.银 | D.铂 |
 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。  )在溶液中呈紫红色。
)在溶液中呈紫红色。
 +4H2O和 。
+4H2O和 。  Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
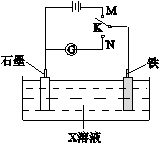
| A.K与N连接时,X为硫酸,一段时间后溶液的pH增大 |
| B.K与N连接时,X为氯化钠,石墨电极反应:2H++2e—=H2↑ |
| C.K与M连接时,X为硫酸,一段时间后溶液的pH增大 |
| D.K与M连接时,X为氯化钠,石墨电极反应:4OH—-4e—=2H2O+O2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com