
A��B��C��D��E��ǰ������ԭ�������������������Ԫ�ء�AԪ��ԭ�ӵĺ����������������Ӳ�����BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ�� A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1:1��2:1��EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�͡���ش����и��⣨�漰Ԫ��������Ӧ��ѧ���ű�ʾ����
��1�� B��C��D����Ԫ���е縺������Ԫ�����̬ԭ�ӵĵ����Ų�ͼΪ ��
��2������һ���ռ��˶�״̬�ĵ�����ԭ�Ӻ�����ֵĸ����ܶȷֲ����� ������������B�Ļ�̬ԭ���У�������� �������෴�ĵ��ӡ�
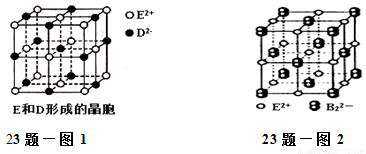
��3����E��D�γɵľ�����ͼ1��ʾ��������E2+��Χ�Ⱦ��������E2+��________����ED����ɫ��ӦΪש��ɫ��������������ǵĻ����ﶼ���Է�����ɫ��Ӧ����ԭ���� ��E��B���γɵľ���ľ����ṹ��NaCl��������ƣ���ͼ2��ʾ�������þ����к��е�������B22���Ĵ��ڣ�ʹ������һ������������������E2+����λ��Ϊ______���û�����ĵ���ʽΪ ��
��4���ø�����������Һ̬Hʱ��һ��H�������ͷų�һ�����ӣ�ͬʱ����һ�������ӡ�
���ͷų����ĵ��ӿ��Ա�����H�����γɵġ�������������ΪH���Ӽ����γɡ�������ԭ���� ��
����H�����ͷų�һ������ʱ������һ�������Ӿ��н�ǿ�������ԣ���д������������SO2��ˮ��Һ��Ӧ�����ӷ���ʽ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʦ���и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������������ѧ�Ŀ�ѧ�һ���˼��������о������N4���ӣ�N4���ӽṹ��ͼ��ʾ����֪����1molN-N����167kJ����������1molN��N�ų�942kJ����������������Ϣ�����ݣ�����˵����ȷ����
A��N4����һ�����͵Ļ�����
B��N4��N2����Ϊͬλ��
C��N4��ѧ���ʱ�N2�ȶ�
D��1molN4������ת��ΪN2���ų�882kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A�������Ʒ���ˮ�У�Na + H2O�� Na+ + OH? + H2��
B��������������NaOH��Һ��SiO2 + 2OH? ��SiO32? + H2O
C�����Ȼ�����Һ�м��������ˮ��Al3+ + 4NH3•H2O��AlO2? + 4NH4+ + 2H2O
D��̼�������Һ��������NaOH��Һ��Ϻ���ȣ�NH4+��OH��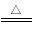 NH3����H2O
NH3����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������人����ʦ��һ����һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ���벻ͬŨ�����ᷴӦʱ�����ֻ�ԭ�������Ժ�����������ҺŨ�ȵĹ�ϵ��������˵������ȷ����
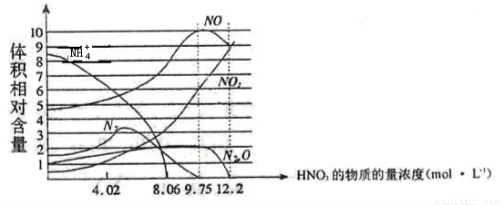
A��һ����˵������������Ӧ�Ļ�ԭ���ﲻ�ǵ�һ��
B����һ�����������������9.75mol��L��1HNO3��Һ��Ӧ�õ���̬������2.24L����μӷ�Ӧ����������ʵ���Ϊ0.1mol.
C�������Ũ��Խ���仹ԭ�����м�̬Խ�ߵijɷ�Խ��
D��������Ũ��Ϊ9.75mol��L��1ʱ��ԭ������NO��NO2��N2O���������ʵ���֮��Ϊ5: 3: 1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������人����ʦ��һ����һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A����������Ҫ��Ⱦ�����CO2��SO2��NO��NO2��O3��
B��PM2.5ָ����ֱ��Ϊ2.5�Ŀ�������������ֱ��С���ȱ��������ǿ���������ж��к������ʣ����˵Ľ����ʹ�������������Ӱ��ϴ�
C���⻯ѧ�������γ��뵪�������йء�
D��SO2�������������豸�У�ԭú���������Ľ�ȼ�ռ��������������豸�ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɳ�и߶��µ��Ĵΰ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪���Դ�С������>̼��>�ӡ����к��廯�����е���ԭ�����ʵ��������¶��ܱ��ǻ�ȡ�������ò����ܸ�NaHCO3��Һ��Ӧ����( )
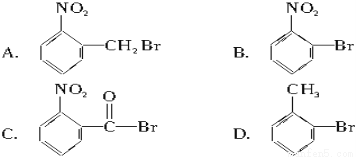
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɳ�и߶��µ��Ĵΰ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ����ʽ�����ӷ���ʽ�У���д��ȷ����( )
A��������ͭ���ڴ�����Һ�У�Cu(OH)2��2H����Cu2����2H2O
B����ȩ��������Ӧ��CH3CHO��Ag(NH3)2OH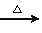 CH3COONH4��NH3��Ag����H2O
CH3COONH4��NH3��Ag����H2O
C����������Һ��ͨ������������̼��C6H5O����CO2��H2O C6H5OH��HCO3��
C6H5OH��HCO3��
D����ϩ�ۺϣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����5���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��������Ũ��Ϊ0.1mol/L��������Һ��pH�����
���� | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 7.5 | 11.6 | 9.7 | 8.3 |
�����й�˵����ȷ���ǣ� ��
A������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��H2CO3��HClO��HF
B������������ʵ���Ũ�ȵ�NaClO��Һ��NaF��Һ������������С��Nǰ��N��
C������CO2ͨ��0.1mol/L Na2CO3��Һ����Һ���ԣ�����Һ�У� 2c��CO32-��+c��HCO3-��= 0.1mol/L
D����Na2CO3��Һ��ͨ��������HF���壬��ѧ��Ӧ����ʽΪ�� Na2CO3 + 2HF = CO2 + H2O + 2NaF
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ��ɶ����и�һ�¿κ���ҵ��ϩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�й�ϩ��������˵���У���ȷ���ǣ� ��
A��ϩ�����������е�ԭ��һ����ͬһƽ����
B��ϩ�������˵�������ֻ�ܷ����ӳɷ�Ӧ���ܷ���ȡ����Ӧ
C������ʽ��C4H8����������һ������̼̼˫��
D��ϩ������ʹ��ˮ��ɫҲ��ʹ����KMnO4��Һ��ɫ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com