
铝可与硝酸钠发生反应:Al+NaNO3+H2O→Al(OH)3↓+N2↑+NaAlO2(未配平),下列有关上述反应的叙述正确的是()
A. 该反应中的氧化剂是水
B. 若反应过程中转移5 mol电子,则生成标准状况下N2的体积为11.2 L
C. 该反应中的氧化产物是N2
D. 当消耗1 mol Al时,生成标准状况下N2的体积为22.4 L
考点: 氧化还原反应;氧化还原反应的计算.
专题: 氧化还原反应专题.
分析: Al+NaNO3+H2O→Al(OH)3↓+N2↑+NaAlO2中,Al元素的化合价升高,N元素的化合价降低,以此来解答.
解答: 解:A.水中H、O元素的化合价不变,则不作氧化剂,故A错误;
B.由N元素的化合价变化+5→0可知,生成1molN2转移10mol电子,则转移5mol电子,则生成标准状况下N2的体积为0.5mol×22.4L/mol=11.2L,故B正确;
C.因N元素的化合价降低,则还原产物为N2,故C错误;
D.由电子守恒可知,10molAl反应生成3molN2,则消耗1molAl时,生成标准状况下N2的体积为0.3mol×22.4L/mol=6.72L,故D错误;
故选B.
点评: 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
在一个1 L的密闭容器中,加入2mol A和1mol B,发生下列反应:2A(g)+B(g)3C(g)+D(s),达到平衡时,C的浓度为1.2mol·L-1。
(1)维持容器的温度不变,若缩小容器的体积,则平衡________
移动(填“向正反应方向”或“向逆反应方向”或“不”)。
(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2mol·L-1的是__________。
A.4mol A+2mol B
B.3mol C+1mol D
C.2mol A+1mol B+1mol D
(3)若维持容器内的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol·L-1,则C的起始物质的量应满足的条件是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A、B、C、D、E、F、G相互关系如图所示。5.2 g F能与100 mL 1 mol·L-1的NaOH溶液恰好完全中和,0.1 mol F还能与足量金属钠反应,在标准状况下放出2.24 L H2。D的分子式为C3H3O2Na,E的分子中含有羧基。
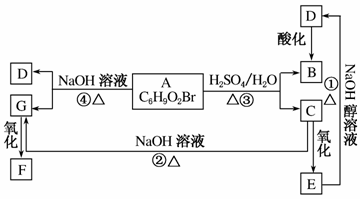
(1)写出下列物质的结构简式:G:________________;F:________________。
(2)化学反应类型:①________________;④________________。
(3)化学方程式:①__________________________;③__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是()
A. 将过量的二氧化碳通入氢氧化钠溶液:CO2+2OH﹣═CO32﹣+H2O
B. 氯化铝溶液中加入过量浓氨水:Al3++4OH﹣═AlO2﹣+2H2O
C. 氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+
D. 碳酸钙和盐酸反应:CO32﹣+2H+═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化钠(NaH)是一种白色的离子晶体,NaH与水反应放出氢气.下列叙述中,正确的是()
A. NaH在水中显酸性
B. NaH中氢离子的电子层排布与氦原子的相同
C. NaH中氢离子半径比锂离子半径小
D. NaH中氢离子可被还原成氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
把Ba(OH)2溶液滴入到明矾溶液中,使SO42﹣全部转化成BaSO4沉淀,此时铝元素的主要存在形式是()
A. Al3+ B. Al(OH)3 C. AlO2﹣ D. Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3.关于该物质的说法正确的是()
A. 该物质属于两性氢氧化物
B. 该物质是Al(OH)3和Na2CO3的混合物
C. 1mol NaAl(OH)2CO3最多可消耗3mol H+
D. 该药剂不适合于胃溃疡患者服用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各反应中属于加成反应的是()
A. C2H4+3O2 2CO2+2H2O
2CO2+2H2O
B. H2+Cl2 2HCl
2HCl
C. CH2=CH2+Br2→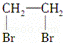
D. CH3﹣CH3+2Cl2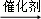 CH2Cl﹣CH2Cl+2HCl
CH2Cl﹣CH2Cl+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中评价合理的是 ( )
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀硝酸反应:2Fe3O4+18H+===6Fe3++H2↑+8H2O | 正确 |
| B | 向碳酸镁中加入稀盐酸:CO | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1∶2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com