
����Ŀ���������б仯�У����ɱ���������������ۻ�����KHSO4���ڣ�����������ˮ������������ˮ����HI�ֽ⡣�������գ�
��1��δ�ƻ���ѧ������_____________����2�������Ӽ����ƻ�����_____________��
��3�������ۼ����ƻ�����_____________��
�����������и������ʣ���ʯī������ϩC60����126C��136C����CH3��CH2��CH2��CH3��CH3��CH��CH3��CH3����Ư�ۺ�Ư��Һ��Ҫ�ɷ֣��������������飻����ϩ�;���ϩ����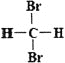 ��
�� ��������ͻ����顣�������գ�
��������ͻ����顣�������գ�
��1��__________������Ϊͬλ������2��__________������Ϊͬ����������
��3��__________����������ͬϵ������4��__________������Ϊͬ���칹����
��5��__________��������ͬһ������
��������A�Ľṹ��ʽΪ��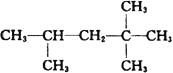 ����������ȼ��Ʒ�ʿ������ܵIJ������ϵͳ��������������_____________________������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ�ֽṹ��ʽΪ��_______________����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ���Ľṹ��ʽΪ__________________��
����������ȼ��Ʒ�ʿ������ܵIJ������ϵͳ��������������_____________________������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ�ֽṹ��ʽΪ��_______________����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ���Ľṹ��ʽΪ__________________��
���𰸡� �٢� �ڢ� �ܢ� �� �� �� �� �� 2��2��4���������� 
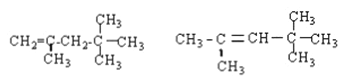
�����������ٸɱ����ڷ��Ӿ��壬����ʱ���ƻ���ѧ�����ƻ����Ӽ����������������Ϊ���Ӿ��壬�ۻ��ƻ��������Ӽ�����KHSO4Ϊ���Ӿ��壬�����ƻ��������Ӽ����������ǹ��ۻ��������ˮ����������Ӻ���������ӣ���������ˮ�ƻ����ǹ��ۼ����������Ƿ��Ӿ��壬����ˮ���ƻ���ѧ�����ƻ����Ӽ�����������HI�ǹ��ۻ�����ֽ�ʱ�ƻ����ǹ��ۼ�����(1)δ�ƻ���ѧ�������٢ݣ�(2)�����Ӽ����ƻ������ڢ�(3)�����ۼ����ƻ������ܢޣ�
��ʯī�ͺ�����ϩC60��ͬһԪ���γɵIJ�ͬ���ʵĵ��ʣ�����Ϊͬ�������壻��126C��136C��ͬһԪ�ص���������ͬ����������ͬ��ԭ�ӣ�����Ϊͬλ�أ���CH3-CH2-CH2-CH3��CH3-CH(CH3)CH3����ʽ��ͬ�ṹ��ͬ����ͬ���칹�壻��Ư�۵���Ҫ�ɷ�Ϊ������ƺ��Ȼ��ƣ���Ư��Һ��Ҫ�ɷ�Ϊ�������ƺ��Ȼ��ƣ�����֮����ϵ���������������鶼���������ṹ���ƣ��ڷ�����������һ�������ɸ�CH2ԭ���ŵĻ������ͬϵ�����ϩ�����Ӿ۷�Ӧ���ɾ���ϩ������ϩ�Ǿ���ϩ�ĵ��壬�����������κι�ϵ�����Ƕ���������ƽ������ֱ�ʾ������ͬһ���ʣ�������������������������ڻ�����������֮����ϵ���ʣ�(1)��������Ϊͬλ����(2)��������Ϊͬ����������(3)������������ͬϵ����(4)��������Ϊͬ���칹����(5)����������ͬһ������
��������A��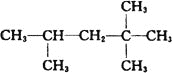 ��ϵͳ�������Ļ�ѧ����Ϊ2��2��4������������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ������Ϊ2��2��3��3-�ļ����飬�ṹ��ʽΪ��
��ϵͳ�������Ļ�ѧ����Ϊ2��2��4������������A��ͬ���칹���к���Ч��ԭ���������ٵ�һ������Ϊ2��2��3��3-�ļ����飬�ṹ��ʽΪ��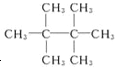 ����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ���Ľṹ��ʽ����Ϊ
����A����ϩ����H2ͨ���ӳɷ�Ӧ�õ������ϩ���Ľṹ��ʽ����Ϊ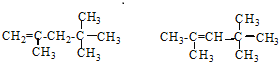 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г��������뽺���ص���
A���峿�������п���һ���ƵĹ���
B�����м��������ʹ�����ʵȾ۳����ƳɿɿڵĶ���
C��FeCl3��Һ����NaOH��Һ�������ɫ����
D�����õ�Ӿ�����ᡢ�齺���������ȵس����ڶƼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��A��B��D��E��G��ԭ������������������A��Gͬ���壬 B��D��Eͬ���ڡ�A�ֱ���B��E��G�γ�ԭ�Ӹ�����Ϊ1:1�Ļ�����ס��ҡ����������� ���³�ѹ�·ֱ�Ϊ���塢Һ�塢���壬��ȼ��ʱ���������Ҳ���Ũ�ҵĺ��̣���Ϊ���Ӿ��塣
(1)D�Ļ�̬ԭ����______��δ�ɶԵ��ӣ��ĵ���ʽΪ____________
(2)����ˮ���ҷ�Ӧ����ǿ��X��A�ĵ��ʣ��仯ѧ����ʽΪ______��
(3)�ҵ�ˮ��Һ�������ԣ�����ˮ�еĵ��뷽��ʽΪ______��
(4)B��E����Ԫ�ذ�ԭ�Ӹ�����1:2�γɻ�����Y����X��Y�����ʵ���֮��Ϊ2:1 ��ȫ��Ӧ��������ҺŨ��Ϊ0.1 mol/L,���и�����Ũ�ȴӴ�С��˳������Ϊ______��
(5)��25��C��10lkPaʱ��16.0gҺ̬D2A4����������ȫȼ�շų�����312 kJ�������� ������Ⱦ���ʣ�����һ��Ϊ���ʣ���һ���������д���÷�Ӧ���Ȼ�ѧ����ʽ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ�е�����Ũ�ȹ�ϵ��ȷ����
A.һ�����ʵ���Ũ�ȵ�Na2S��Һ����c(OH��)��c(H��)��2c(H2S)��c(HS��)
B.������ˮ�м������NaOH��c(Na��)��c(Cl��)��c(ClO��)��c(OH��)
C.pH��8.3��NaHCO3��Һ��c(Na��)>c(HCO3-)>c(CO32-)>c(H2CO3)
D.25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L��1��CH3COOH��CH3COONa�����ҺpH��4.75��
c(![]() )+c(
)+c(![]() )=c(CH3COOH)+c(H+)
)=c(CH3COOH)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʹ������к͵ζ����ⶨ���۰״�������(g��100mL��1)��
��.ʵ�鲽��
(1)����100ml����״���Һ:�� (����������)��ȡ10.00 mLʳ�ð״ף����ձ�����ˮϡ�ͺ�ת�Ƶ� (����������)�ж��ݣ�ҡ�ȼ��ô���״���Һ��
(2)����ʽ�ζ���ȡ����״���Һ20.00 mL����ƿ�У������еμ�2�� ��ָʾ����
![]()
(3)��ȡʢװ0.1000 mol��L��1 NaOH ��Һ�ļ�ʽ�ζ��ܵij�ʼ���������Һ��λ����ͼ��ʾ�����ʱ�Ķ���Ϊ________mL��
(4)�ζ�����___________________________ʱ��ֹͣ�ζ�������¼NaOH��Һ���ն������ظ��ζ�3�Ρ�
��.ʵ���¼
�ζ�����ʵ������(mL) | 1 | 2 | 3 | 4 |
V(��Ʒ) | 20.00 | 20.00 | 20.00[ | 20.00 |
V(NaOH)(����) | 15.95 | 15.00 | 15.05 | 14.95 |
��.���ݴ���������
(1)��ʵ���������ݣ��ɵ�c(���۰״�)�� mol��L��1��
���۰״��������� g��100 mL��1��
(2)�ڱ�ʵ��ĵζ������У����в�����ʹʵ����ƫ�����________��д���)��
a����ʽ�ζ����ڵζ�ʱδ�ñ�NaOH��Һ��ϴ
b����ʽ�ζ��ܵļ����ڵζ�ǰ�����ݣ��ζ���������ʧ
c����ƿ�м������״���Һ���ټ�����ˮ
d����ƿ�ڵζ�ʱ����ҡ����������Һ�彦��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ǣ� ��
A.�������һ���ܼӿ췴Ӧ����
B.�¶�Խ�߷�Ӧ����ҲԽ��
C.���������СҲ��Ӱ�췴Ӧ����
D.��Ӧ������Ҫ�ɷ�Ӧ�����ʾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ������һЩ��ѧ���ļ��ܣ����ݼ������ݹ��㷴ӦCH4��g��+4F2��g��=CF4��g��+4HF��g���ķ�Ӧ����HΪ����������
��ѧ�� | C��H | C��F | H��F | F��F |
����/��kJmol��1�� | 414 | 489 | 565 | 155 |
A. +485 kJmol��1 B. ��485 kJmol��1
C. +1940 kJmol��1 D. ��1940 kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʣ�����������ʡ������˳�����е���( )
A. �ռҺ̬������� B. ��ʯ�ҡ����ס���ʯ��
C. �ɱ��������Ȼ��� D. ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������pH��������ȷ���ǣ� ��
A.��7
B.��5.6
C.��5.6��7֮��
D.����5.6
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com