
【题目】设 NA为阿伏加德罗常数的值,下列说法不正确的是( )
A. 5mL0.1mol/LKI 溶液和 1mL0.1mol/LFeCl3 溶液充分反应,转移电子数小于 0.0001NA
B. 标准状况下, 2.24LCH4、 C2H4 混合气体完全燃烧,消耗的氧气分子数为 0.25NA
C. 常温常压下, 100g 质量分数为 46%的乙醇水溶液中含有的氧原子数为 4 NA
D. 6g 二氧化硅晶体中含有的硅氧键数为 0.4NA
【答案】B
【解析】2Fe3++2I-![]() 2Fe2++I2,该反应为可逆反应,进行不到底,转移电子数小于 0.0001NA,A正确;2.24LCH4、 C2H4 混合气体为0.1 mol,若气体全为0.1 mol CH4,完全燃烧消耗的氧气分子数为0.2NA,若气体全为0.1 mol C2H4,完全燃烧消耗的氧气分子数为0.3NA,所以消耗的氧气分子数为在0.2NA与0.3NA 之间,不一定为0.25NA,B错误;100g 质量分数为 46%的乙醇中含有的氧原子数为100×46%÷46×NA= NA;水中含有氧原子数为(100-100×46%)÷18×NA=3 NA,所以乙醇溶液中含有的氧原子数为 4NA,C正确;1 mol二氧化硅晶体含有4 mol硅氧键,6g 二氧化硅晶体(即为0.1mol)含有的硅氧键数为 0.4NA,D正确;正确选项B。
2Fe2++I2,该反应为可逆反应,进行不到底,转移电子数小于 0.0001NA,A正确;2.24LCH4、 C2H4 混合气体为0.1 mol,若气体全为0.1 mol CH4,完全燃烧消耗的氧气分子数为0.2NA,若气体全为0.1 mol C2H4,完全燃烧消耗的氧气分子数为0.3NA,所以消耗的氧气分子数为在0.2NA与0.3NA 之间,不一定为0.25NA,B错误;100g 质量分数为 46%的乙醇中含有的氧原子数为100×46%÷46×NA= NA;水中含有氧原子数为(100-100×46%)÷18×NA=3 NA,所以乙醇溶液中含有的氧原子数为 4NA,C正确;1 mol二氧化硅晶体含有4 mol硅氧键,6g 二氧化硅晶体(即为0.1mol)含有的硅氧键数为 0.4NA,D正确;正确选项B。


科目:高中化学 来源: 题型:
【题目】已知A在通常状况下是一种相对分子质量为28的气体,其产量通常用来衡量一个国家的石油化工水平。B、D是饮食中两种常见的有机物,现以A为主要原料合成一种具有果香味的乙酸乙酯F,F中碳原子数是D的两倍。其合成路线如下图所示。
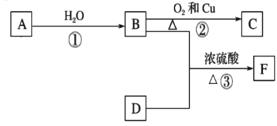
请回答下列问题:
(1)写出A的分子式为________,A中的所有原子是否共平面 ______(填“是”或“否”)。
(2)B、 D分子中的官能团名称分别是____________、 _____________。
(3)写出下列反应的化学方程式,并指出反应类型:
反应①:__________________________;___________。
反应②:__________________________;___________。
反应③:__________________________;___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应为N2O(g)+CO(g) CO2(g)+N2(g) △H,有关化学反应的物质变化过程(图1)及能量变化过程(图2)如下:
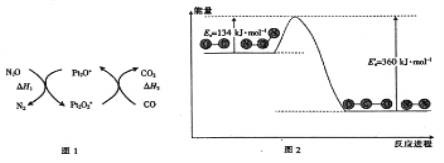
下列说法正确的是( )
A.由图1可知:△H1=△H+△H2
B.由图2可知△H =-226 kJ/mol
C.为了实现转化需不断向反应器中补充Pt2O+和Pt2O2+
D.由图2可知该反应正反应的活化能大于逆反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4–)+ c(C2O42–)=0.100 mol·L–1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A.pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)>c(HC2O4–)
B.c(Na+)=0.100 mol·L–1的溶液中:c(H+)+c(H2C2O4)=c(OH–)+c(C2O42–)
C.c(HC2O4–)=c(C2O42–)的溶液中:c(Na+)>0.100 mol·L–1+c(HC2O4–)
D.pH=7的溶液中:c(Na+)<2c(C2O42–)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A 气体为直线型分子;B、C气体在标况下的密度均为1.25g/L;反应①②反应机理类似且原子利用率均为 100%;请回答下列问题:

(1)D 中含有的官能团的名称为________________________;
(2)高分子涂料 H 的结构简式为________________________;
(3)下列说法正确的是(___)
A.鉴别有机物 A、 C 可以选用溴的四氯化碳溶液,褪色的是 A
B.反应⑤既是加成反应,又是还原反应,而且原子利用率为 100%
C.高分子涂料 H 含有碳碳双键,所以可以使酸性高锰酸钾溶液褪色
D.反应③④中浓硫酸的作用为催化剂和吸水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是( )
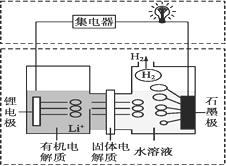
A. 石墨极发生的反应是2H2O+2e— === H2↑+2OH—
B. 有机电解质和水溶液不可以互换区域
C. 该装置不仅可提供电能,还可得到清洁的氢气
D. 标准状况下产生22.4 L的氢气时,正极消耗锂的质量为14 g
【答案】D
【解析】A、根据图示信息可知,石墨电极上产生H2,则石墨电极为正极,电极反应为:2H2O+2e=H2↑+2OH,故A正确;B、Li和有机电解质不反应,而Li和水反应,若Li和水接触,会有部分化学能直接转化为热能,所以有机电解质和水溶液不可以换区域,故B正确;C、该原电池是将化学能转化为电能的装置,装置不仅可提供电能,并且反应产物是氢气,能提供氢能源,故C正确;D、金属锂是负极,故D错误。故选D。
【题型】单选题
【结束】
26
【题目】一种新型的“锂-呼吸CO2电池”,结构如图所示,下列说法不正确的是
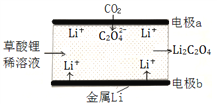
A. 该装置是化学能转变为电能
B. 利用该技术可减少温室气体CO2的排放
C. 正极的电极反应为:2CO2 + 2e- = C2O42-
D. 每生成10.2g Li2C2O4,有0.2mol Li+从正极迁移至负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com