
下列图示与对应的叙述相符的是
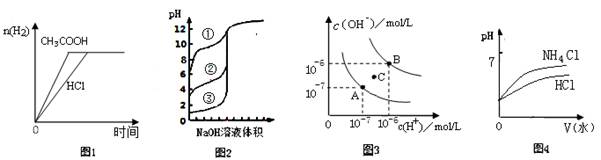
A.图1中曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中,分别加入足量镁粉,产生H2的物质的量的变化
B.图2表示用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由曲线可确定③的酸性最强
C.图3为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
D.图4表示将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数时,二者 pH的变化
B
【解析】
试题分析:醋酸是弱酸,盐酸是强酸,在物质的量浓度相等的条件下,盐酸和镁的反应速率快,所用时间少,A不正确;B中根据曲线可知,消耗氢氧化钠的体积是相同的,这说明三种酸的浓度是相同的。但③的pH最小,说明③的酸性最强,B正确;C中,从A点到C点水的离子积常数是增大的,所以改变的条件应该是升高温度,C不正确;稀释促进氯化铵的水解,氢离子的物质的量增加,所以在稀释过程中氯化铵溶液的pH应该小于盐酸的,D不正确,答案选B。
考点:考查弱电解质的电离、酸碱中和滴定、水的离子积常数以及盐类水解
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力。该题的关键是明确各种平衡状态的特点以及外界条件对平衡状态的影响,然后结合图像,灵活分析、判断即可。


科目:高中化学 来源: 题型:
A、图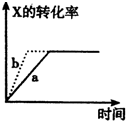 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 | B、图 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 | C、图 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 | D、图 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com