
【题目】氮和碳的化合物与人类生产、生活密切相关。
(1)已知:N2(g)+O2(g)===2NO(g); ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g); ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH=__________。
(2)在压强为0.1 MPa条件,将CO和H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
①下列能说明该反应达到平衡状态的是________________。
a.混合气体的密度不再变化 b.CO和H2的物质的量之比不再变化
c.v(CO)=v(CH3OH) d.CO在混合气中的质量分数保持不变
②T1℃时,在一个体积为5 L的恒压容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.75,则T1℃时,CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=_______________________。
CH3OH(g)的平衡常数K=_______________________。

③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当![]() 时,达到平衡状态,CH3OH的体积分数可能是图象中的___________点。
时,达到平衡状态,CH3OH的体积分数可能是图象中的___________点。
(3)用催化转化装置净化汽车尾气,装置中涉及的反应之一为:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
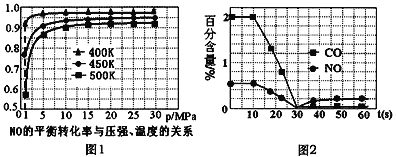
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到如图1所示的曲线。催化装置比较适合的温度和压强是___________。
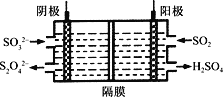
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图2所示。则前10 s内,CO和NO百分含量没明显变化的原因是____________。
(4)如图所示的装置能吸收和转化NO2和SO2。
①阳极区的电极反应式为___________________________。
②阴极排出的溶液中含S2O![]() 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO![]() 可在阴极区再生。写出该反应的离子方程式:___________________________。
可在阴极区再生。写出该反应的离子方程式:___________________________。
【答案】 -664.1 kJ·mol-1 ad 75 F 400K,1Mpa 尚未达到催化剂工作温度或尚未达到反应所需的温度 SO2-2e-+2H2O===SO![]() +4H+ 4S2O
+4H+ 4S2O![]() +2 NO2+8OH-=8SO
+2 NO2+8OH-=8SO![]() +N2+4H2O
+N2+4H2O
【解析】(1)根据盖斯定律:第二个方程式减第一个方程式,整理后即可计算出该反应的ΔH= -664.1 kJ·mol-1;正确答案:-664.1 kJ·mol-1。
(2)①在压强不变的情况下,反应前后混合气体的总质量不发生改变,气体的总体积在发生变化,当二者的比值不再发生改变时,反应达到平衡状态,a正确;CO和H2都为反应物,在发生反应时是按照1:2比例进行的,无 论 进 行 到 什 么 程 度,二 者的物质的量之比不再变化,无法判断反应是否达平衡,b错误;v(CO)=v(CH3OH)没 有 标 出 速 率 的方向,无法判定,c错误;反应达到平衡状态后,CO在混合气中的质量分数保持不变,d正确。答案选ad。
② 因为CO的转化率为0.75,所 以 反应 中 消 耗 CO的 总 量为 0.75 mol,容器的体积为5 L。
CO(g) + 2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始量 1 2 0
变化量 0.75 1.5 0.75
平衡量 0.25 0.5 0.75
平衡浓度0.05 0.1 0.15
平衡常数=  ,正确答案:300。
,正确答案:300。
③温度不变,当![]() 时, 甲醇的体积分数为最大值, 当
时, 甲醇的体积分数为最大值, 当![]() 时,虽然增加了氢气的浓度,平衡右移,甲醇的含量增加,但是混合气体的总体积增加的多,导致CH3OH的体积分数减少,应该是图象中的F点;正确选项F。
时,虽然增加了氢气的浓度,平衡右移,甲醇的含量增加,但是混合气体的总体积增加的多,导致CH3OH的体积分数减少,应该是图象中的F点;正确选项F。
(3)①根据图像可知,在压强不变的情况下,该反应温度越低,NO的转化率越大;当反应温度在400K时,压强为1 Mpa时,转化率为90%,当压强增大到5 Mpa时,转化率为95%,虽然转化率有提高,但是压强的增大,需 要 很 高 的 成本,不划算,所以催化装置比较适合的温度和压强是400K、1Mpa;答案为400K、1Mpa。
②需要控制在一定的温度范围内,才能发挥催化剂的最大催化能力,则前10 s内,尚未达到催化剂工作温度或尚未达到反应所需的温度,所以CO和NO百分含量没明显变化;正确答案:尚未达到催化剂工作温度或尚未达到反应所需的温度。
(4)①阳极发生氧化反应,SO2失去电子被氧化为硫酸,根据电子守恒、电荷守恒、原子守恒规律,极反应为SO2-2e-+2H2O===SO![]() +4H+ ;正确答案为 SO2-2e-+2H2O==SO
+4H+ ;正确答案为 SO2-2e-+2H2O==SO![]() +4H+。
+4H+。
②在碱性环境中,S2O![]() 离子中+3价硫元素被氧化为+4价的SO
离子中+3价硫元素被氧化为+4价的SO![]() ,NO2中+4价的氮元素被还原到0价,即为氮气,无污染气体,离子方程式为4S2O
,NO2中+4价的氮元素被还原到0价,即为氮气,无污染气体,离子方程式为4S2O![]() +2 NO2+8OH- = 8SO
+2 NO2+8OH- = 8SO![]() +N2
+N2
+4H2O ; 正确答案:4S![]() +2 NO2+8OH- =8SO
+2 NO2+8OH- =8SO![]() +N2+4H2O 。
+N2+4H2O 。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】硫酸锰在电解锰、染料、造纸以及陶瓷等工业生产中有广泛的应用。利用软锰矿(主要成分为MnO2,含铁的化合物等杂质)和闪锌矿(主要成分ZnS)制得硫酸锰的流程如下:
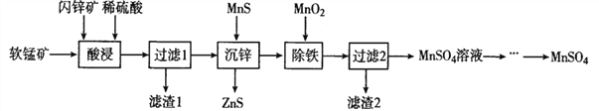
(1)“酸浸”时,为了缩短浸取时间,常加入少量FeSO4溶液,FeSO4的作用可能是___________________;MnO2、ZnS及硫酸反应转变为两种硫酸盐的化学方程式为______________________。
(2)常温下,Ksp(ZuS)=1.2×l0-24、Ksp(MnS)=1.5×10-15,“沉锌”反应为:Zn2+(aq)+MnS![]() ZnS+Mn2+(aq),该反应的平衡常数K=__________________。
ZnS+Mn2+(aq),该反应的平衡常数K=__________________。
(3)在强酸性条件下加入MnO2氧化Fe2+的离子方程式为___________________。
(4)“除铁”时需要调节pH约为3~4,过滤所得的滤渣2中除MnO2以外的另一种物质是________________。(写化学式)
(5)该工艺流程中可以循环利用的物质是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于吸热反应的是 ( )
A.铝跟盐酸反应B.酒精的燃烧
C.盐酸与氢氧化钠溶液的反应D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会可持续发展密切相关。下列做法错误的是
A.利用风力发电,减少CO2的排放
B.为提高粮食产量,大量使用高残留农药
C.对秸秆进行加工,使其转化为汽车燃料
D.按照国家规定,对生活垃圾进行分类放置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
(1)烃A的分子式为__________.
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则燃烧时消耗标准状况下的氧气____________L.
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为_____________.
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式有三种,它们分别为________、________、_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系:
![]()
(1)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_______________。
②A溶液一步转化为C溶液的反应离子方程式为________________。
(2)若X是一种黄绿色的气体,Y的饱和溶液滴入沸水中能生成红褐色胶体。
①检验溶液Z是否变质最灵敏的一种试剂是____________________(名称);
②一定条件下W与水反应的化学方程式_______________________________。
(3)X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法____________________,X转化为Y的化学方程式为______________________;
(4)X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为________________________________________;
②请画出向含0.01molX和0.01molY的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O==HClO+HSO3-
B. 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合: Al3++2SO42-+2Ba2++4OH- =2BaSO4+AlO2-+ 2H2O
C. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
D. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H+ +2I-=2Fe2+ +I2 +3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请参考题中图表,已知E1=134kJ/mol、E2=368kJ/mol,根据要求回答问题:
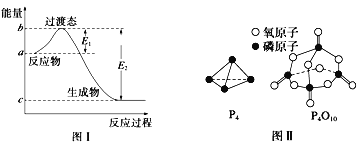
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能最变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___(填“增大”、“减小”或“不变”下同),△H的变化是________。请写出NO2和CO反应的热化学方程式:__________。
(2)如表所示是部分化学键的键能参数:
化学键 | P-P | P-O | O=O | P=O |
键能/kJ/mol | a | b | c | x |
已知白磷的燃烧热为dkJ/mol,白磷及其完全燃烧的产物的结构如图II所示。1个P4O10分子中P-O的个数为_______,表中x=_____kJ/mol(用含a、b、c、d的代表数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com