
| A. | 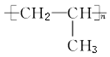 | B. | 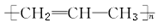 | ||
| C. | 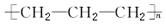 | D. | 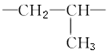 |
科目:高中化学 来源: 题型:解答题
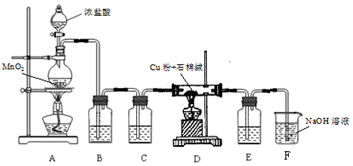
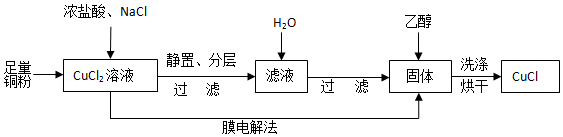
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
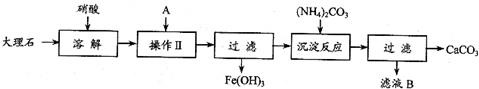
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①表示2molC(s)燃烧生成2molCO(g)需要吸收221 kJ的热量 | |
| B. | 碳的燃烧热大于110.5 kJ/mol | |
| C. | 稀硫酸与浓NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
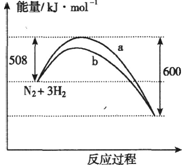
| A. | 该反应的热化学方程式为:N2+3H2?2NH3△H=-92kJ•mol-1 | |
| B. | a曲线是加入催化剂时的能量变化曲线 | |
| C. | 加入催化剂,该化学反应的反应热改变 | |
| D. | 在温度体积一定的条件下,通入1mol N2和3 mol H2反应后放出的热量为69kJ,则N2的转化率为75% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.3℃ | -56.8kJ/mol |
| ② | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散系的分类: 分散系微粒直径 分散系微粒直径 | |
| B. | 溶液是电中性的,而胶体是带电的 | |
| C. | 光线通过时,溶液产生丁达尔效应,胶体则无丁达尔效应 | |
| D. | 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com