
| A. | 加入稀盐酸产生无色气体,原物质一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入稀盐酸后再加入硝酸银,产生白色沉淀,则原溶液一定有Cl- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,不一定有Ba2+ |
分析 A.可能含有HCO3-;
B.可能生成AgCl沉淀;
C.加入盐酸,不能确定原溶液是否含有氯离子;
D.可能为BaCO3、CaCO3、MgCO3等白色沉淀.
解答 解:A.加入盐酸产生无色气体,将气体通入石灰水中,溶液变浑浊,说明生成二氧化碳气体,溶液中可能含有HCO3-或CO32-等离子,故A错误;
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,沉淀可能为AgCl,应先加入盐酸,如无现象,再加入氯化钡检验,如生成沉淀,则说明含有硫酸根离子,故B错误;
C.加入盐酸,不能确定原溶液是否含有氯离子,应加入硝酸酸化,故C错误;
D.可能为BaCO3、CaCO3、MgCO3等白色沉淀,所以不一定为Ba2+,故D正确.
故选D.
点评 本题考查物质的检验、鉴别,为高考常见题型,侧重于学生的分析、实验和评价能力的考查,注意把握离子的性质以及实验的合理性、可行性的评价,题目难度中等.


科目:高中化学 来源: 题型:解答题

 .
.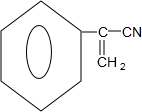 ,E中含氧官能团的名称为羧基.
,E中含氧官能团的名称为羧基. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| B. | 向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全Ba2++H++OH-+SO42-=BaSO4↓+H2O | |
| C. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3- | |
| D. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液2Fe2++2H++H2O2=2Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol | B. | 0.25 mol | C. | 0.27 mol | D. | 0.52 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ .写出C与NaOH水溶液共热反应的化学方程式
.写出C与NaOH水溶液共热反应的化学方程式 +3NaOH$→_{△}^{水}$
+3NaOH$→_{△}^{水}$ +2NaBr+H2O.
+2NaBr+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,A在周期表中的位置为第三周期ⅢA族.
,A在周期表中的位置为第三周期ⅢA族.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实 验 操 作 | 答案 | 实验现象 |
| (1)向鸡蛋清中滴加少许浓硝酸,微热 | B | A.紫色褪去 B.变黄色 C.出现蓝色 D.溶液分层,下层呈紫红色 |
| (2)将乙烯通入少量酸性KMnO4溶液中 | A | |
| (3)将CCl4滴入盛有碘水的试管中,充分振荡,静止 | D | |
| (4)向土豆片上滴加碘水 | C |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 ,反应类型加聚反应;
,反应类型加聚反应;
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4的摩尔质量(g/mol)与NA个硫酸分子的质量(g)在数值上相等 | |
| B. | NA个氧气分子和NA个氮气分子的质量比为8:7 | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 1mol D2(重氢分子)中含有2NA个中子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com