
| A. | 裂化汽油不能用于萃取溴水中的溴 | |
| B. | 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体异构)4种 | |
| C. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| D. | 油脂在碱性条件下的水解反应称为皂化反应 |
分析 A、裂化汽油中含烯烃;
B、分子式为C5H10O2且与NaHCO3溶液能产生气体,则该有机物中含有-COOH,所以为饱和一元羧酸,烷基为-C4H9,丁基异构数等于该有机物的异构体数;
C、钠也能和乙醇反应;
D、油脂在碱性条件下水解为硬质酸钠.
解答 解:A、裂化汽油中含烯烃,故能和溴发生加成反应,不能用于萃取溴水中的溴,故A正确;
B、分子式为C5H10O2且与NaHCO3能产生气体,则该有机物中含有-COOH,所以为饱和一元羧酸,烷基为-C4H9,-C4H9异构体有:-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-CH2CH(CH3)CH3,-C(CH3)3,故符合条件的有机物的异构体数目为4,故B正确;
C、钠也能和乙醇反应生成氢气,故不能用钠检验乙醇中是否含水,故C错误;
D、油脂在碱性条件下水解为硬质酸钠,是肥皂的主要成分,故油脂在碱性条件下的水解为皂化反应,故D正确.
故选C.
点评 本题主要考查同分异构体书写、官能团的性质与确定等,侧重于学生的分析能力的考查,难度中等,熟练掌握碳原子数小于5的烃基的个数是解决本题的关键,甲基与乙基均1种,丙基2种、丁基4种、戊基8种.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
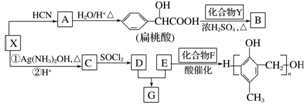
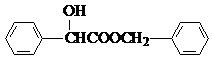 .
.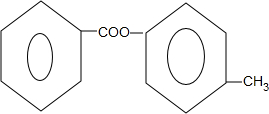 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$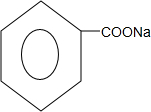 +
+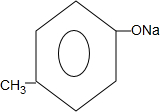 +H2O.
+H2O.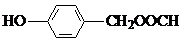 ,
,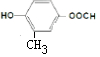 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子的半径:W>X>Z | |
| B. | 最简单气态氢化物的稳定性:W>Z>Y | |
| C. | 最高价氧化物对应水化物的酸性:Z>Y>X | |
| D. | W与Y形成的化合物中只含共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用水浴加热法控制温度 | |
| B. | 采用边反应边蒸馏的方法提高产率 | |
| C. | 制取装置中有冷凝回流措施 | |
| D. | 用水和氢氧化钠溶液洗涤后分液分离出产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;B与E形成的化合物
;B与E形成的化合物 ;A、B、E形成的化合物Na+
;A、B、E形成的化合物Na+ ;D、E形成的化合物
;D、E形成的化合物 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
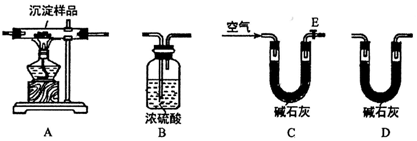
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X为IA族时,Y不可能是第三周期VIA族元素 | |
| B. | 由X、Y、Z、W四种元素不可能形成其原子个数比为1:3:1:1的化合物 | |
| C. | Z元素的原子半径一定小于W元素的原子半径 | |
| D. | 若X为IVA族元素时,X、Y两元素可形成含有共价键的离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com