
| A.可能等于7 | B.一定<7 | C.一定>7 | D.无法判断 |
科目:高中化学 来源:不详 题型:计算题
 淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为:
淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为: 算过程)
算过程)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.2 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.⑤⑥⑦⑧ | C.③⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| ① | ② | ③ | ④ |
| 0.1mol/L CH3COOH溶液 | pH = 12 NaOH溶液 | 0.1mol/L NaOH溶液 | pH = 2 CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
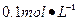 Na2SO3溶液,正确的是
Na2SO3溶液,正确的是| A.升高温度,溶液的pH降低 |
| B.c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3) |
| C.c(Na+)+c(H+)="2" c(SO32―)+ 2c(HSO3―)+ c(OH―) |
| D.加入少量NaOH固体,c(SO32―)与c(Na+)均增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤ | B.①②③④ | C.①③⑤ | D.②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com