
| 选项 | 实验目的 | 实验操作 | 实验原理 |
| A | 用普通酒精精制无水酒精 | 加入硫酸铜,蒸馏 | 硫酸铜吸水 |
| B | 除去乙醇中少量乙酸 | 加入钠,分液 | 乙酸与钠反应 |
| C | 分离甲酸丙酯和丙酸甲酯 | 蒸馏 | 它们的沸点不同 |
| D | 除去硝基苯中少量稀酸溶液 | 加入石油醚,萃取 | 石油醚溶解硝基苯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.无水硫酸铜可检验水的存在,不能分离提纯;
B.乙醇、乙酸均与Na反应;
C.二者互溶,但沸点不同;
D.加入石油醚,硝基苯中引入石油醚新杂质.
解答 解:A.无水硫酸铜可检验水的存在,不能分离提纯,应加CaO、蒸馏分离,故A错误;
B.乙醇、乙酸均与Na反应,不能除杂,应选碳酸钠、蒸馏,故B错误;
C.二者互溶,但沸点不同,则蒸馏可分离,故C正确;
D.加入石油醚,硝基苯中引入石油醚新杂质,应加碳酸钠溶液、分液,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意有机物性质与混合物分离提纯的结合,题目难度不大.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:多选题
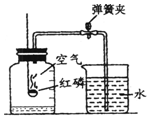 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )| A. | 该实验证明空气中氧气的质量分数约占$\frac{1}{5}$ | |
| B. | 实验时红磷要足量 | |
| C. | 实验前一定要检查装置的气密性 | |
| D. | 红磷燃烧的火焰熄灭后立刻打开弹簧夹 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
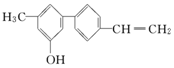
| A. | 完全燃烧时只有二氧化碳和水两种产物 | |
| B. | 由于含有氧元素不是有机物 | |
| C. | 该分子中含有羟基属于醇 | |
| D. | 不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
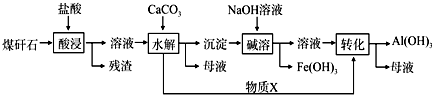
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乳酸是一种纯净物 | |
| B. | 聚乳酸的聚合方式与聚苯乙烯相似 | |
| C. | 聚乳酸的单体为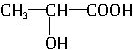 | |
| D. | 聚乳酸的降解过程不需要其他物质参与反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸亚铁溶液中加入双氧水的离子方程式:Fe2++2H2O+4H+=Fe3++4H2O | |
| B. | 粗硅制备的化学方程式:C+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Si | |
| C. | 石墨作电极电解CuSO4溶液的离子方程式:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 铁发生吸氧腐蚀时负极上的电极反应式:Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
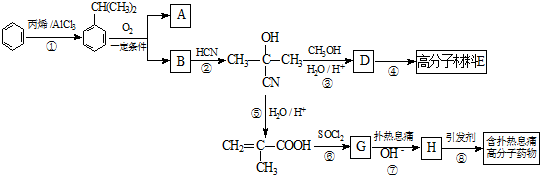
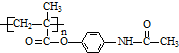 .
.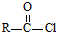
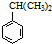 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com