
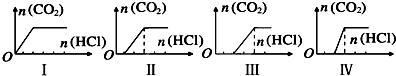


科目:高中化学 来源: 题型:
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发):

则下列分析都正确的组合是
| 溶液组成主要成分 | 对应图象 | 溶液中离子浓度关系 | |
| A | NaHCO3 | I | c(Na+) = c(HCO3-) |
| B | NaHCO3、Na2CO3 | Ⅱ | c(CO32-) < c(HCO3-) |
| C | NaOH、Na2CO3 | Ⅲ | c(OH-) > c(CO32-) |
| D | Na2CO3 | Ⅳ | c(Na+) = c(CO32-) + c(HCO3-) + c(H |
查看答案和解析>>
科目:高中化学 来源: 题型:
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,可以得到不同的成分组合,其中混合组分的物质的量为1:1 请选择下列分析都正确的组合是:
|
| 溶液组成主要成分 | 溶液中离子浓度关系 |
| A | NaHCO3、Na2CO3 | c(CO32-) < c(HCO3-) |
| B | NaOH 、 Na2CO3 | c(OH-)<c(CO32-) |
| C | Na2CO3 | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D | NaHCO3、NaOH | c(Na+) = c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,可以得到不同的成分组合,其中混合组分的物质的量为1:1 请选择下列分析都正确的组合是:
|
|
溶液组成主要成分 |
溶液中离子浓度关系 |
|
A |
NaHCO3、Na2CO3 |
c(CO32-) < c(HCO3-) |
|
B |
NaOH 、 Na2CO3 |
c(OH-)<c(CO32-) |
|
C |
Na2CO3 |
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
|
D |
NaHCO3、NaOH |
c(Na+) = c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
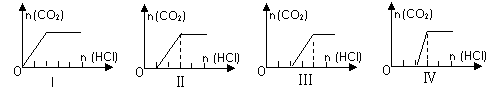
(09上海奉贤区4月模拟)向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:
![]()
![]()
![]()
![]() 则下列分析都正确的组合是:
则下列分析都正确的组合是:
| 溶液组成主要成分 | 对应图象 | 溶液中离子浓度关系 |
A | NaHCO3、Na2CO3 | Ⅱ | c(CO32-) < c(HCO3-) |
B | NaOH 、 Na2CO3 | Ⅲ | c(OH-)>c(CO32-) |
C | Na2CO3 | Ⅳ | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
D | NaHCO3 | I | c(Na+) = c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,可以得到不同的成分组合,其中混合组分的物质的量为1:1 请选择下列分析都正确的组合是:
| 溶液组成主要成分 | 溶液中离子浓度关系 | |
| A | NaHCO3、Na2CO3 | c(CO32-) < c(HCO3-) |
| B | NaOH 、 Na2CO3 | c(OH-)<c(CO32-) |
| C | Na2CO3 | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D | NaHCO3、NaOH | c(Na+) = c(HCO3-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com