
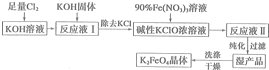

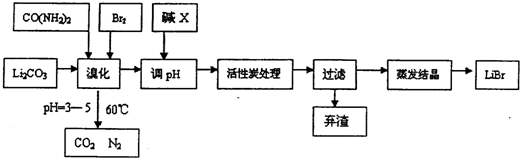
���� ����Cl2ͨ���KOH��Һ�У��¶ȵ�ʱ������ӦCl2+2OH-=Cl-+ClO-+H2O������ҺI�м���KOH��ʹ������ȫ��Ӧ���ҽ���Һת��Ϊ������Һ��ֻ�м��������´���������Ӳ��ܺ������ӷ���������ԭ��Ӧ���ɸ���������ӣ���ȥKCl�õ����Ե�KClOŨ��Һ������Ե�KClOŨ��Һ�м���90%��Fe��NO3��3��Һ��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���õ���ҺII�������õ�ʪ��Ʒ����ʪ��Ʒϴ�ӡ�����õ�����K2FeO4��
��1���ɹ������̼��ۿ�֪������Fe��NO3��3��KClO�Ʊ�K2FeO4������Ϣ�ڿ�֪�¶Ƚϸ�KOH��Cl2 ��Ӧ���ɵ���KClO3��
��2����ҵ�����õ�ⱥ��ʳ��ˮ��ȡ������
��3�������Ӻʹ���������ӷ���������ԭ��Ӧ���ɸ���������ӣ���ϵ���غ㡢�����غ���д��
��4���ɹ������̿�֪����ӦҺI���й�����Cl2��Ӧ�����ɸ����KClO��
��5������2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���㣻
��6����Na2FeO4����������ˮ��ԭ��������������ԣ�������ɱ��������Fe3+�γɽ��壬��������������ľ�ˮ�����ã����ʱ����Feʧ���ӷ���������Ӧ���缫��Ӧ����ʽΪFe+8OH--6e-�TFeO42-+4H2O��
������H2O2������ԭ��Ӧ���õ����ӱ���ԭ����OH-��
��� �⣺����Cl2ͨ���KOH��Һ�У��¶ȵ�ʱ������ӦCl2+2OH-=Cl-+ClO-+H2O������ҺI�м���KOH��ʹ������ȫ��Ӧ���ҽ���Һת��Ϊ������Һ��ֻ�м��������´���������Ӳ��ܺ������ӷ���������ԭ��Ӧ���ɸ���������ӣ���ȥKCl�õ����Ե�KClOŨ��Һ������Ե�KClOŨ��Һ�м���90%��Fe��NO3��3��Һ��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���õ���ҺII�������õ�ʪ��Ʒ����ʪ��Ʒϴ�ӡ�����õ�����K2FeO4��
��1���ɹ������̼��ۿ�֪������Fe��NO3��3��KClO�Ʊ�K2FeO4������Ϣ�ڿ�֪�¶Ƚϸ�KOH��Cl2 ��Ӧ���ɵ���KClO3������Ϣ�ٿ�֪���ڵ�����KOH��Cl2 ��Ӧ���ɵ���KClO����ѡ����½ϵͣ��ʴ�Ϊ���¶Ƚϵͣ�
��2����ҵ�����õ�ⱥ��ʳ��ˮ��ȡ��������Ӧ����ʽΪ��2NaCl+2H2O $\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2�����ʴ�Ϊ��2NaCl+2H2O $\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����
��3�����������ǿ�����ԣ��۽���������������Ϊ������������ӷ���ʽ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5 H2O��
�ʴ�Ϊ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5 H2O��
��4���ɹ������̿�֪����ӦҺI���й�����Cl2��Ӧ����KOH�����Ŀ�����������Cl2������Ӧ�����ɸ����KClO��
A���������Cl2������Ӧ�����ɸ����KClO����A��ȷ��
B������Ϣ�ڿ�֪�¶Ƚϸ�KOH��Cl2 ��Ӧ���ɵ���KClO3��������KClO���ɡ��˷�ԭ�ϣ���B����
C���ɹ������̼��ۿ�֪������Fe��NO3��3��KClO�Ʊ�K2FeO4����C��ȷ��
D������Ϣ��֪����������KClO3 ����ת��ΪKClO����D����
�ʴ�Ϊ��AC��
��5��n��K2FeO4��=$\frac{59.4g}{198g/mol}$=0.3mol������2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O֪�������������ʵ���=$\frac{0.3mol}{2}$=0.45mol��
������Ϊ0.45mol��90.5g/mol=40.73g��
�ʴ�Ϊ��40.73��
��6����Na2FeO4����������ˮ��ԭ��������������ԣ�������ɱ��������Fe3+�γɽ��壬��������������ľ�ˮ�����ã����ʱ����Feʧ���ӷ���������Ӧ���缫��Ӧ����ʽΪFe+8OH--6e-�TFeO42-+4H2O���ʴ�Ϊ��Fe+8OH--6e-�TFeO42-+4H2O��
��NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ�������H2O2������ԭ��Ӧ���õ���������OH-����缫��ӦΪ��H2O2+2e-=2OH-���ʴ�Ϊ��H2O2+2e-=2OH-��
���� ���⿼�����ʵ��Ʊ�ʵ�鷽������ƣ�Ϊ�߿��������ͣ���Ŀ��Ƕȿ���ѧ���Ķ���Ŀ��ȡ��Ϣ���������Թ������̵������������Ŀ��ơ�ԭ��غ͵���ԭ���ȣ����ؿ���ѧ������������������˼ά���������Ѷ��еȣ���Ҫѧ��������ʵ�Ļ���֪ʶ���������֪ʶ��������������ע�����֪ʶ�����գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 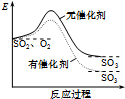 ��ͼ��ʾSO2������Ӧ�ֱ����С�����������·�Ӧ�����е������仯 | |
| B�� | 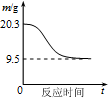 ��ͼ��ʾ0.1 mol MgCl2•6H2O�ڿ����г�ּ���ʱ����������ʱ��ı仯 | |
| C�� | 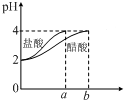 ��ͼ��ʾ�ֱ�ϡ��10 mL pH=2������ʹ���ʱ��ҺpH�ı仯��ͼ��b��100 | |
| D�� | 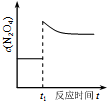 ��ͼ��ʾƽ��2NO2��g��?N2O4��g����t1ʱѸ�ٽ������С��c��N2O4���ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 | |
| 1 | �� | �� | ||||||
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧ�����ȷ�Ӧ����A������̬ | B�� | ����Ӧ�Ƿ��ȷ�Ӧ����A������̬ | ||
| C�� | ����Ӧ�����ȷ�Ӧ����A����̬ | D�� | ����Ӧ�Ƿŷ�Ӧ����A����̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�����������ڲ��ܺϳɵ����� | B�� | �л��ﶼ�Ǻ���̼Ԫ�صĻ����� | ||
| C�� | �л������ﶼ��ȼ�� | D�� | ����̼Ԫ�ص����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �屽�е��壨KI��Һ�� | B�� | �����е���ϩ�����Ը�����أ� | ||
| C�� | ���������е����ᣨ����Na2CO3��Һ�� | D�� | ���еļױ���Br2ˮ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com