
| A. | 浓硫酸可刻蚀石英制艺术品 | |
| B. | 活性炭、SO2和Na2O2都具有漂白作用,且漂白的化学原理相同 | |
| C. | 石油的裂化、煤的气化、Na2FeO4杀菌消毒均属于化学变化 | |
| D. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 |
分析 A.浓硫酸与二氧化硅不反应;
B.活性炭利用吸附性漂白、SO2和有色物质化合生成无色物质、Na2O2利用强氧化性漂白;
C.石油的裂化主要得到烷烃和烯烃、煤的气化生成CO和氢气、Na2FeO4杀菌消毒利用强氧化性;
D.水玻璃为硅酸钠的水溶液,PM2.5微粒直径大于胶体中分散质的直径.
解答 解:A.浓硫酸与二氧化硅不反应,应利用HF酸刻蚀石英制艺术品,故A错误;
B.活性炭利用吸附性漂白、SO2和有色物质化合生成无色物质、Na2O2利用强氧化性漂白,原理不同,故B错误;
C.石油的裂化主要得到烷烃和烯烃、煤的气化生成CO和氢气、Na2FeO4杀菌消毒利用强氧化性,均发生化学变化,故C正确;
D.水玻璃为硅酸钠的水溶液,PM2.5微粒直径(2.5×10-6m)大于胶体中分散质的直径(10-7m~10-9m),不具有丁达尔现象,而氢氧化铁溶胶、淀粉溶液均具有丁达尔效应,故D错误;
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.


科目:高中化学 来源: 题型:解答题
 HClO
HClO
 Mg
Mg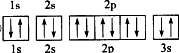 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+ | Al3+ | Fe3+ | Cu2+ | Ba2+ |
| 阴离子 | OH- | Cl- | CO32- | NO3- | SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外有38个电子,核内有95个质子 | B. | 核外有38个电子,核内有57个中子 | ||
| C. | 核外有57个电子,核内有57个质子 | D. | 核外有57个电子,核内有38个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
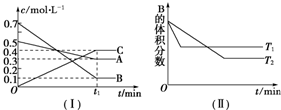
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com