
| A. | 一定温度和压强下,气态物质的体积主要由构成气体的分子的大小决定 | |
| B. | 从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液中氢离子的浓度为4mol/L | |
| C. | 同温同压下,30mLA2气体和10mL B2气体恰好完全反应生成20mLC气体,则C化学式为 A3 B或B A3 | |
| D. | 同温同压下任何气体的分子间距离几乎相等 |
分析 A.一定温度和压强下,气态物质的体积主要由气体分子数目多少决定;
B.溶液是均匀的,取出溶液浓度与原溶液浓度相等;
C.同温同压下,气体体积之比等于其物质的量之比,结合原子守恒确定C的化学式;
D.一定温度和压强下,气体间距约是相等的.
解答 解:A.由于气体分子大小远远小于气体间距,气体分子大小可以忽略,一定温度和压强下,气体间距约是相等的,故一定温度和压强下,气态物质的体积主要由气体分子数目多少决定,故A错误;
B.硫酸溶液中氢离子的浓度为2mol/L×2=4mol/L,溶液是均匀的,取出溶液浓度与原溶液浓度相等,从1 L 2 mol/L的H2SO4溶液中取出的0.5 L溶液中氢离子的浓度为4mol/L,故B正确;
C.同温同压下,气体体积之比等于其物质的量之比,则发生反应:3A2+B2=2C,由原子守恒可知C化学式为 A3B或BA3,故C正确;
D.同温同压下,任何气体的分子间距离几乎相等,故D正确,
故选:A.
点评 本题考查气体摩尔体积、物质的量浓度等,比较基础,注意对基础知识的理解掌握.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
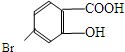 ,它的含氧官能团名称为羧基、羟基.
,它的含氧官能团名称为羧基、羟基.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学小组采用类似制乙酸乙酯的装置(如图),用环己醇制备环己烯.
化学小组采用类似制乙酸乙酯的装置(如图),用环己醇制备环己烯.
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 难溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 碱 | 盐 | 氧化物 | |
| A | 硫 酸 | 纯 碱 | 硫酸钡 | 水 |
| B | 氢硫酸 | 烧 碱 | 纯 碱 | 石灰石 |
| C | 碳 酸 | 熟石灰 | 小苏打 | 二氧化硫 |
| D | 二氧化碳 | 苛性钾 | 食 盐 | 石灰石 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化还原反应的实质是电子的得失 | |
| B. | 氧化还原反应中得、失电子的总数一定相等 | |
| C. | 有单质参加的反应一定是氧化还原反应 | |
| D. | 氧化还原反应中一定有氧原子的得到与失去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高 | B. | 降低 | C. | 不变 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2009年2月21日,法国佳士得拍卖行“伊去•圣洛朗与皮埃尔•贝尔热珍藏”专物拍卖会拍卖品预展在法国巴黎大皇宫拉开帷幕.25日,中国圆明园流失文物鼠首和兔首铜像被拍卖.普通铜器的时间稍久容易出现铜绿,其主要成分是Cu2(OH)2CO3.这两件铜铸的国宝仍然熠熠生辉不生锈,下列对其主要原因的分析,最可能的是( )
2009年2月21日,法国佳士得拍卖行“伊去•圣洛朗与皮埃尔•贝尔热珍藏”专物拍卖会拍卖品预展在法国巴黎大皇宫拉开帷幕.25日,中国圆明园流失文物鼠首和兔首铜像被拍卖.普通铜器的时间稍久容易出现铜绿,其主要成分是Cu2(OH)2CO3.这两件铜铸的国宝仍然熠熠生辉不生锈,下列对其主要原因的分析,最可能的是( )| A. | 它们的表面都镀上了一层耐腐蚀的黄金 | |
| B. | 环境污染日趋严重,它们表面的铜绿被酸雨溶液溶解洗去 | |
| C. | 铜的金属活动性比氢小,因此不易被氧化 | |
| D. | 它们是含一定比例金、银、锡、锌的铜合金 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com